体内では、血管を通じて様々な物質が運ばれ、生命活動が維持されています。血管はまさに「体内の道路」といえる存在です。
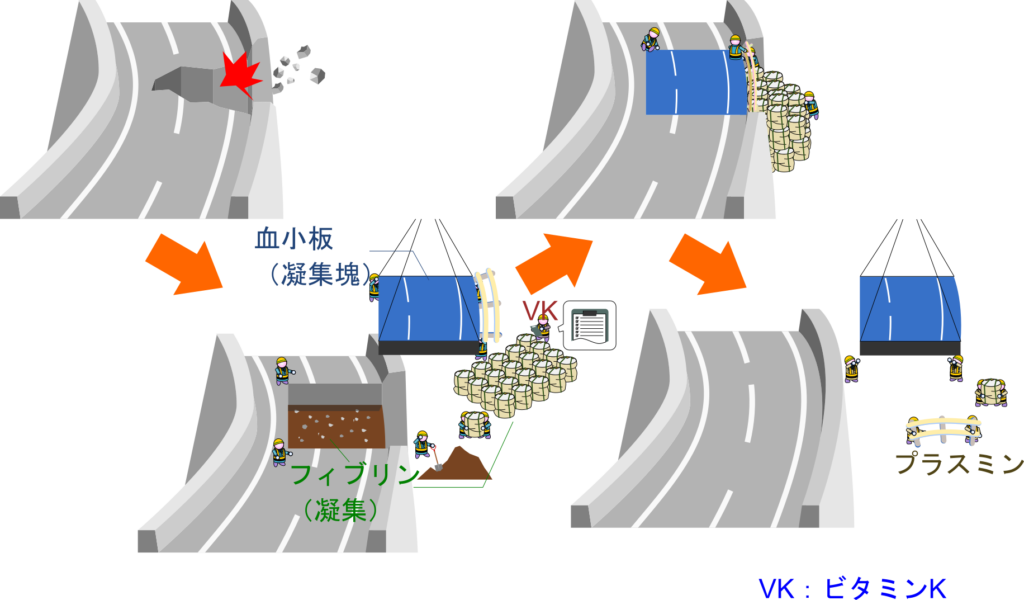
もし道路が損傷すれば、まずは仮設道路を設置して通行を確保し、その後に本格的な修復が行われ、最後に仮設物は撤去されます。図で示すように、体内でも同様のプロセスが働いています。
血管が損傷すると、血小板が集まって応急的に傷口をふさぎ(一次止血)、続いてフィブリンが網目構造を形成して強固に固定します(二次止血)。そして組織の修復が完了すると、プラスミンによってフィブリンは分解され、元の状態へと戻ります。
ここで重要なのがビタミンK です。ビタミンK は凝固因子をカルボキシル化し、Ca²⁺を介して損傷部位に集積できる状態にすることで、これらの反応を効率的に進行させます。言い換えれば、ビタミンKは「止血を成立させるための準備を整える分子」です。
本記事では、ビタミンKの種類や構造から出発し、γ-カルボキシグルタミン酸(Gla)の生成機構、さらに血液凝固メカニズムや凝固カスケードの反応機序、凝固カスケードにおけるビタミン K の役割までを体系的に解説します。
Contents
ビタミンKの種類と構造
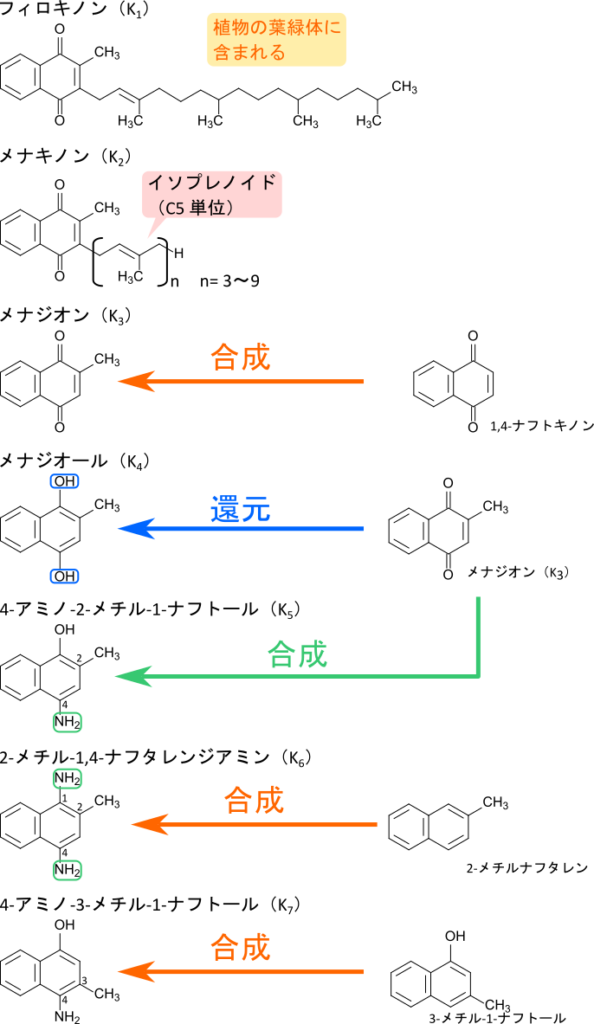
天然のビタミンKには植物の葉緑体に含まれるビタミンK1(フィロキノン;phylloquinone)と微生物の生産物であるビタミンK2(メナキノン;menaquinone)が存在します。さらにメナキノンには側鎖の長さによっていくつかの種類が存在します。メナキノンの側鎖は(炭素数5の)イソプレン単位の繰り返しとなっており、イソプレン単位の数によってメナキノン-4 やメナキノン-7 などと呼ばれています。この他にもビタミンKと同等の作用を有する合成化合物があり(図 1)、これらの化合物はビタミンKと同様のキノン骨格を持つ点で共通しています。
構造からわかるように天然のビタミンK は脂溶性のビタミンですが、一部の合成ビタミンK は水酸基やアミノ基が付加されていることや疎水性の側鎖がないことから、水溶性が天然のビタミンK より高くなっています。また、ほかの脂溶性ビタミンや脂質と同様に吸収はミセルを介して行われ、キロミクロンに取り込まれたのちに肝臓へ輸送されます。肝臓では VLDL(Very Low-Density Lipoprotein)に取り込まれて血中に放出され、末梢細胞へ輸送されます。
ビタミンKによるグルタミン酸のカルボキシル化:γ-カルボキシグルタミン酸(Gla)生成
ビタミン K による Gla 生成
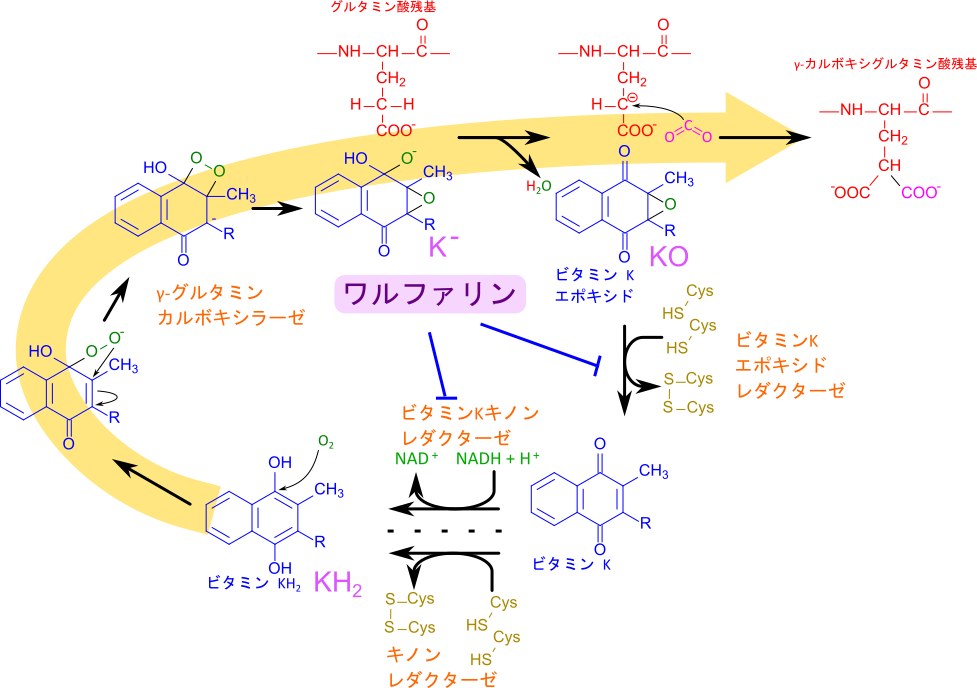
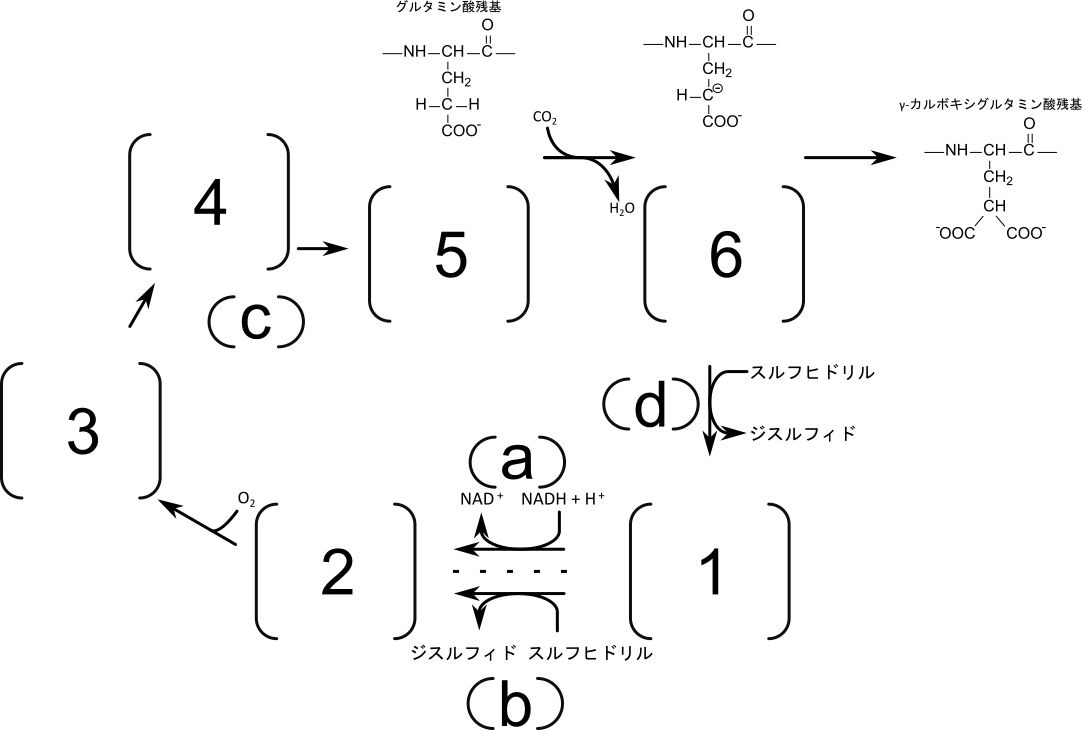
ビタミンKの最も重要な機能の一つがグルタミン酸のカルボキシル化です。ビタミン K はビタミン K レダクターゼやキノンレダクターゼの機能により還元型ビタミンK(KH2)に変換されます。KH2 は酸素化されて K– へ変換されます(図2)。この K– は強い塩基であり、グルタミン酸の γ 炭素が脱プロトン化されて、カルボアニオンとなり、非酵素的に CO2 が付加されて γ カルボキシグルタミン酸が生成される一方で、K– はビタミンKエポキシド(KO)に変換されます。KO はビタミン K エポキシドレダクターゼの作用によりビタミン K へ還元されます。この作用は2つのチオール基がジスルフィド結合へ酸化される反応と共役しています(図2)。
ビタミン K 阻害剤による Gla 生成阻害
この反応はワルファリンにより阻害されます。ワルファリンの存在下ではビタミン K エポキシドの還元やビタミン K キノンの還元が阻害されます。このうち、ビタミン K がヒドロキノン(KH2)になる過程にはワルファリンによって阻害を受ける経路と阻害を受けない経路が知られています(ワルファリン非感受性経路の責任酵素については研究が進められています)。このため、ワルファリンの存在下ではビタミン K エポキシドが蓄積されて排泄され、γ-カルボキシグルタミン酸の生成が抑制されます(図2)。
ビタミン K 阻害剤と血液凝固作用の阻害
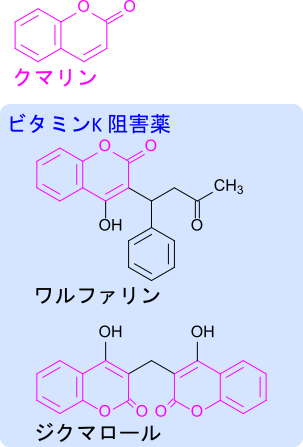
ビタミンKの発見の契機は腐敗した牧草を食べたウシで出血を伴う症状が発生し、死亡したことでした。この原因はジクマロール(Dicumarol)という物質であることがわかりました。ジクマロールはクマリン誘導体が会合した構造を持つ分子でビタミン K の作用を阻害します。ビタミン K 依存性凝固系因子であるVII、IX、X、II はビタミン K によって Gla が導入され、血液凝固作用において重要な役割を担います。ウシの例ではビタミン K の作用が阻害されたことで血液凝固が上手く機能できずに発生した現象でした。このことを参考に抗凝固製剤のワルファリン(Warfarin)が開発されています。ワルファリンはクマリン構造を含む分子で、Gla の生成を阻害します。
γ-カルボキシグルタミン酸残基(Gla 残基)の凝固における役割
ビタミン K は γ-カルボキシグルタミン酸残基の生成において重要な役割を担います。この機能は凝固系でも鍵となる機能です。実際、ビタミン K の発見はビタミン K の機能阻害による凝固系の機能不全でした。そこで、ここでは凝固系の作用機序を確認し、γ-カルボキシグルタミン酸残基がどのように関与するかを解説します。
凝固系は血小板の反応と凝固カスケードがあり、これらが協調的に作用することで効率的な止血を達成しています。まずはそれぞれの反応について詳しく見ていきましょう。
凝固系における血小板の機能
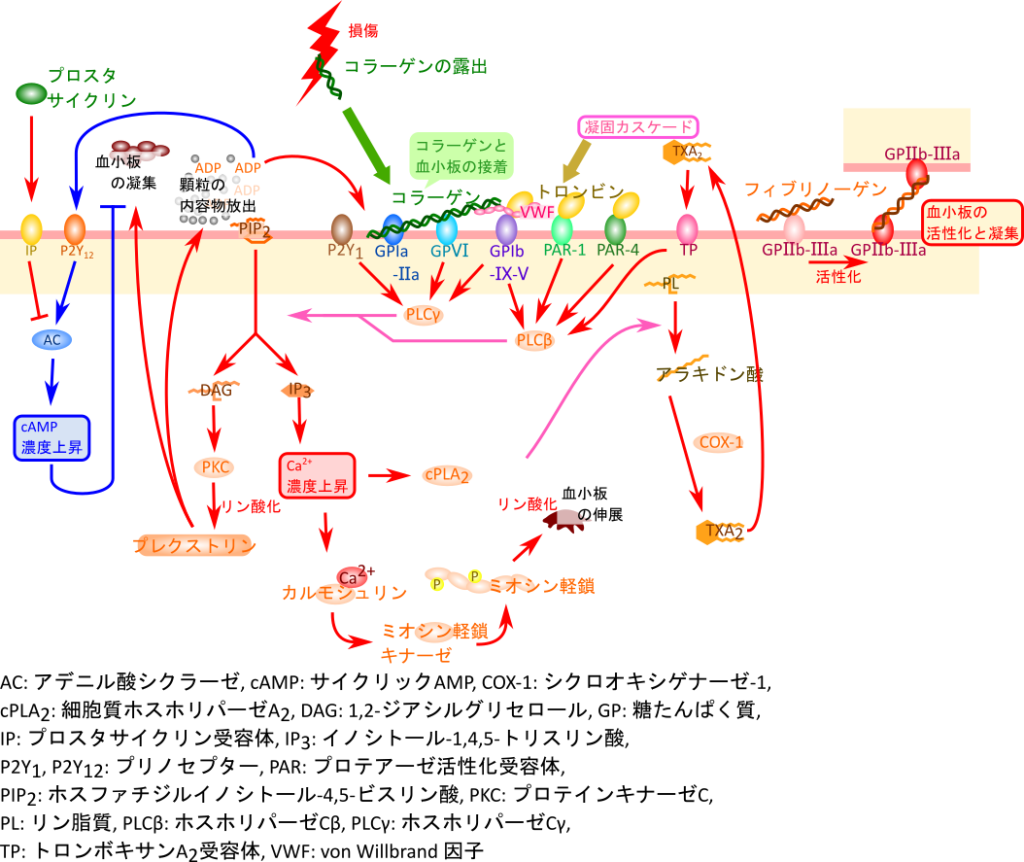
創傷などにより(普段は血液と隔離されている)コラーゲンが露出すると血小板膜糖タンパク質(glycoprotein; GP)Ia-IIa 複合体 や GPⅣ (CD36) などが露出したコラーゲンを認識してホスホリパーゼCγ(PLCγ)を活性化してホスファチジルイノシトール-4,5-ビスリン酸(PIP2)を1.2‐ジアシルグリセロール(DAG)とイノシトール-1,4,5-トリスリン酸(IP3)に分解します。この反応は創傷などにより放出が誘導されるフォンビルブランド因子(von Wilbrand factor; VWF)が GPIb-IX-V 複合体に認識されることでも誘導されます。DAG や IP3 は細胞内のセカンドメッセンジャーであり、DAG はプロテインキナーゼC(PKC)を活性化する一方で IP3 は細胞内 Ca2+濃度の上昇を誘導します。
まずは DAG のシグナルについて見ていきましょう。DAG に活性化された PKC はプレクストリン(pleckstrin)をリン酸化して活性化し、血小板の凝集を誘導するほか、顆粒の内容物を放出します。放出される分子の中には ADP も含まれており、プリノレセプター(P2Y1)を刺激して PLCγ によるシグナルを増幅します。
一方、IP3 により Ca2+ 濃度が上昇するとカルモジュリンが Ca2+ と結合し、ミオシン軽鎖を活性化して血小板の伸展を誘導します。また細胞質ホスホリパーゼA2(cPLA2)はリン脂質を加水分解してアラキドン酸を放出させます。アラキドン酸はシクロオキシゲナーゼ-1(COX-1)によりプロスタグランジンH2(PGH2)を経てトロンボキサンA2(TXA2)に変換されます。トロンボキサンA2 は薬理メディエーターであり、血小板から放出されるとトロンボキサンA2 受容体(TP)に認識されます。TP はホスホリパーゼβ(PLCβ)を活性化しますが、この分子も PLCγ 同様ホスファチジルイノシトール-4,5-ビスリン酸(PIP2)の加水分解を触媒し、シグナルを増幅します。
これらの反応はコラーゲン以外にも凝固カスケードからもたらされるトロンビンによっても誘導されます。トロンビンはプロテアーゼ活性化受容体(proteinase activation receptor; PAR)-1 や -4 などに認識され、PLCβ の活性化とそれに続くホスファチジルイノシトール-4,5-ビスリン酸(PIP2)の加水分解を誘導します。
このように、血小板はコラーゲン、VWFやトロンビン(凝固カスケード)からのシグナルを受け取って血小板の凝集や伸展を引き起こし、効率的な止血に寄与します。
凝固カスケード
凝固カスケードには内因性と外因性があり、内因性は創傷部位で露出した負に荷電した活性化表面(DNA、RNA、ポリリン酸など)により開始され、外因性では血管外に普段は存在し、創傷を受けると血液と接触する組織因子(tissue factor; TF)によって開始されます。
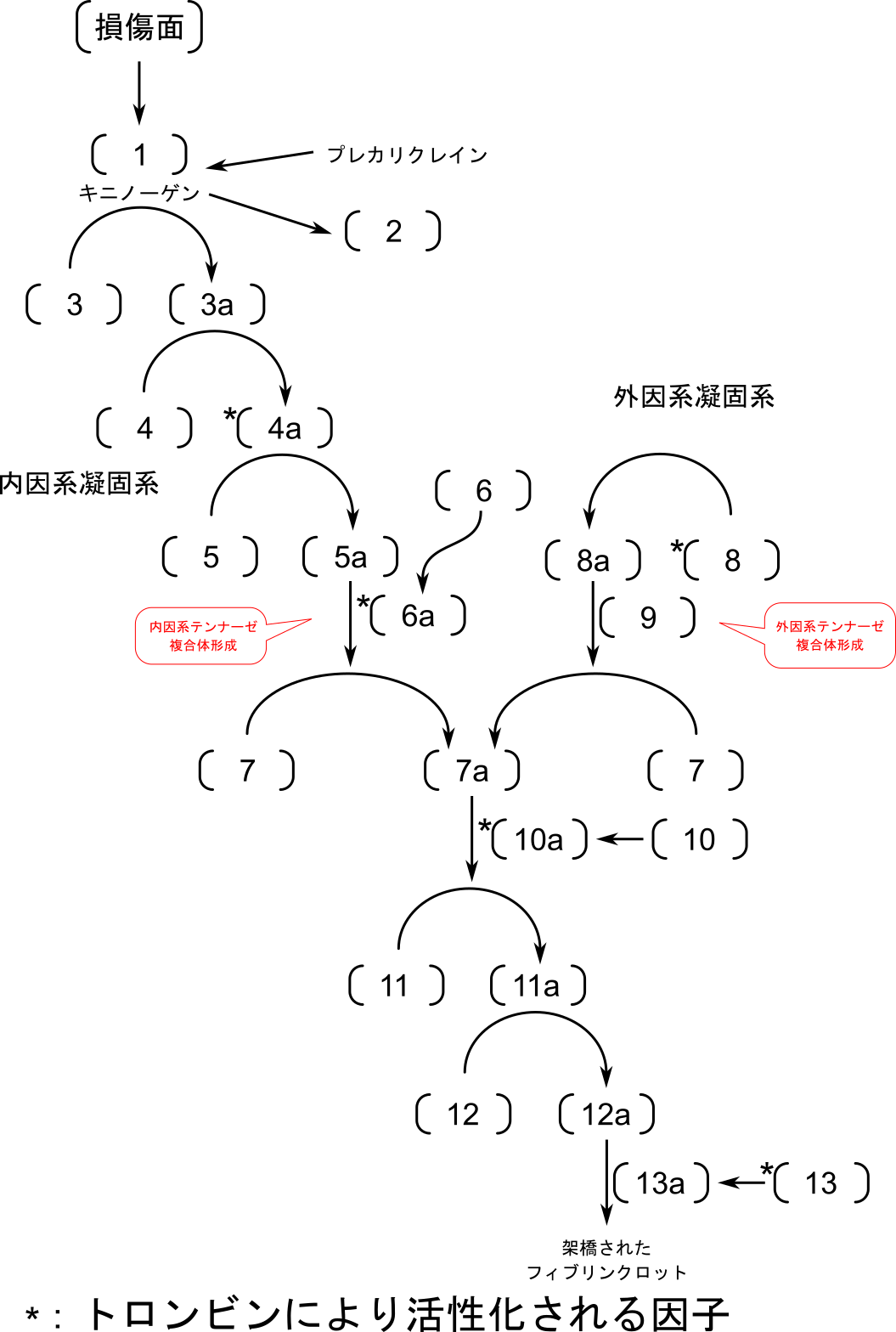
内因性凝固系カスケードでは、凝固第XII因子(以下、凝固第・・因子は単に・・と記載します)が活性化・切断されて XIIa となります。XIIa はプレカリクレインを活性化してカリクレインに変換し、カリクレインはキニノーゲンをブラジキニンへ変換し、血管拡張作用を及ぼします。一方で、XIIa は XI を活性化・切断して XIa に変換します。さらに XIa は IX を活性化し、IXa に変換します。IXa は VIIIa と Ca2+ と内因性テンナーゼ複合体を形成します。この複合体は X を活性化して Xa に変換し、Va と複合体を形成してプロトロンビンをトロンビンへ変換します。トロンビンはフィブリノーゲンをフィブリンに変換・活性化してフィブリンの凝集を引き起こし、XIIIa によって安定化されます。
外因性凝固カスケードでは VII がCa2+、組織因子(TF)と複合体(外因性テンナーゼ複合体)を形成して活性化し、X が活性化されます。この段階で内因性凝固カスケードと合流し、以下同様に反応経路が進行していきます。
カスケードに関与する因子の内、いくつかはカスケードの促進に寄与します。XIIa はプレカリクレインのカリクレインへの変換に対して正の制御を発揮し、自身の産生を促進します。VIIa は外因性凝固カスケードの因子でありながら、内因性凝固カスケードの IX の活性化を促進します。トロンビンはフィードバック・フィードフォワード制御の重要な因子で XI、VIII、V の活性化の他に、XIII の活性化も促進し、凝固カスケードの亢進に寄与します。また、「凝固系における血小板の機能」でも解説したように、トロンビンは血小板の活性化にも関与し、創傷時の止血に中心的な役割を果たします。
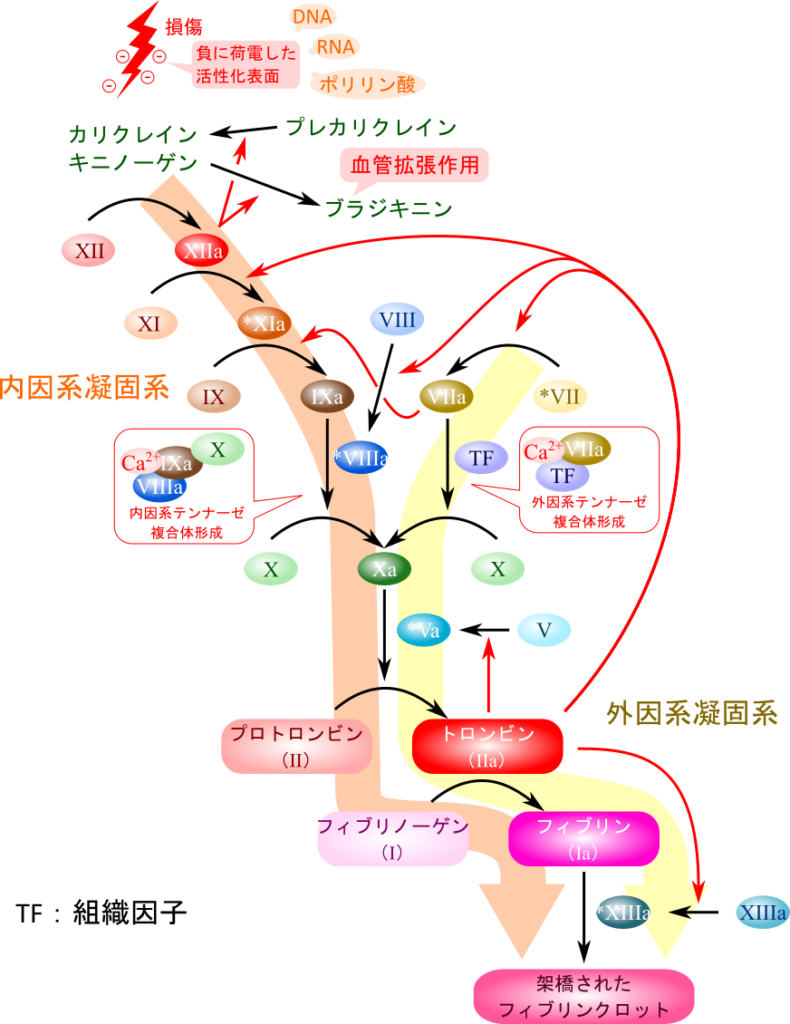
a: 血液凝固因子の活性化型、*: トロンビンにより活性化される因子
| 因子番号 | 分子名(英語) |
|---|---|
| 凝固第 I 因子 | フィブリノーゲン(Fibrinogen) |
| 凝固第 II 因子 | プロトロンビン(Prothrombin) |
| 凝固第 III 因子 | 組織因子(Tissue factor) |
| 凝固第 IV 因子 | Ca2+ |
| 凝固第 V 因子 | プロアクセレリン(Proaccelerin) |
| 凝固第 VI 因子 | 欠番/凝固第 V 因子の活性化型 |
| 凝固第 VII 因子 | プロコンバーチン(Proconvertin) |
| 凝固第 VIII 因子 | 抗血友病因子A(Antihemophilic factor A) |
| 凝固第 IX 因子 | クリスマス因子(Christmas factor) |
| 凝固第 X 因子 | スチュアート・プロウェア因子(Stuart–Prower factor) |
| 凝固第 XI 因子 | Plasma Thromboplastin Antecedent;PTA |
| 凝固第 XII 因子 | ハーゲマン因子(Hageman factor) |
| 凝固第 XIII 因子 | フィブリン安定化因子(Fibrin stabilizing factor) |
代表的な凝固因子の因子番号と分子名を示す。()内は英語名を示すが、英語名のみの場合は()は省略している。なお、凝固第 VI 因子は凝固第 V 因子の活性化型であることが判明したため、現在は欠番とされる。
フィブリンの凝固メカニズム
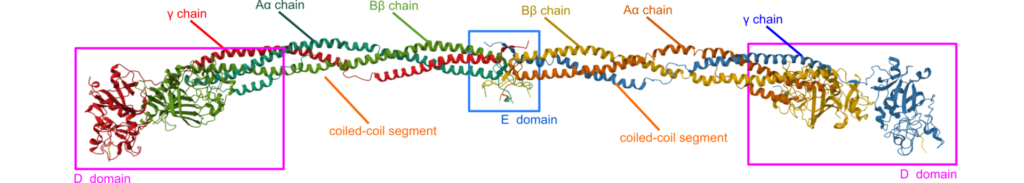
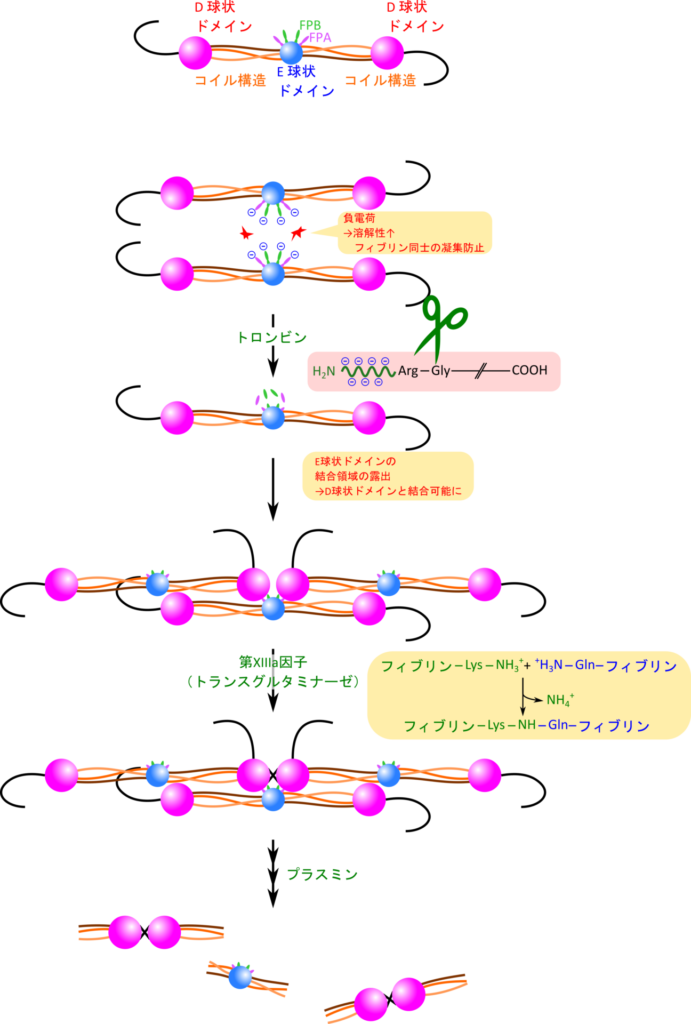
フィブリノーゲンはAα鎖、Bβ鎖、γ鎖それぞれ2本ずつの計6本がヘテロ二量体を形成しています。フィブリノーゲンのドメイン構造は中央にE球状ドメイン、両端にD球状ドメインを持っており、これらの間を三本鎖のコイル構造がつないでいます(図 6)。EドメインにはフィブリノペプチA鎖(Aα鎖の一部; FPA)とフィブリノペプチトB鎖(Bβ鎖の一部; FPB)と呼ばれる領域があり、通常は強く負に帯電して反発しあい、フィブリノーゲンが凝集することを防いでいます。トロンビンは FPA と FPB を切断してフィブリノーゲンをフィブリンに変換し、フィブリン同士の凝集を可能にします。フィブリン同士が凝集すると XIIIa の作用でリシン残基の側鎖アミノ基(-NH2)とグルタミンの側鎖のカルボキサミド基(-CO-NH2)間が架橋されます。このようにしてフィブリンは凝集して強固な架橋構造を形成し、血液を凝固させます。最終的に、創傷部位が治癒してフィブリンが必要なくなるとプラスミンの作用によりフィブリンが分解され、除去されます。
凝固系とビタミンK
凝固系因子のうち、II、VII、IX、Xはビタミン K 依存性です。これらの因子が Gla 化されることで、Ca2+とともに血小板表面のホスファチジルセリンに結合することができるようになります。これらの凝固系因子が活性化されるとセリンプロテアーゼ(活性中心にセリンを利用する酵素)として機能しますが、ホスファチジルセリンはこれらの凝固系因子と結合して集積することで、速やかな凝固カスケードの進行を可能にしています。
トロンビンは凝固カスケードの中でも凝固カスケードの増幅を担っています。ビタミン K 依存性因子であるプロトロンビンは活性化されてトロンビンとなるとフィブリノーゲンの活性化や血小板の活性化など凝固系において中心的な役割を担っています。また、Xa はトロンビンの活性化を、VIIa や IXa による Xa の活性化ステップはカスケード上流因子の活性化の鍵となる段階です。凝固カスケードにおいてカギとなるこれらの因子の活性に関与している点で、ビタミン K は凝固系において重要な栄養素であることがわかります。
ビタミンKの骨形成における役割
ビタミン K は骨形成においても重要な役割を担っていることが知られています。骨形成は、骨芽細胞がコラーゲン繊維とプロテオグリカンを生成し、Ca2+を沈着させてヒドロキシアパタイトを形成することで進行します。この過程において骨芽細胞はオステオカルシン(osteocalcin)を産生し、オステオカルシンのハイドロキシアパタイトへの結合を介してハイドロキシアパタイト結晶の形状や大きさを調整すると考えられています。オステオカルシンは1分子当たり3つの γ-カルボキシグルタミン酸残基(Gla)を持っており、ビタミン K はこの γ-カルボキシグルタミン酸の導入に関与しており、Ca2+ との親和性の向上に寄与していると考えられています。
練習問題
本記事では、ビタミンKの構造と種類から出発し、γ-カルボキシグルタミン酸(Gla)の生成機構、さらに血液凝固カスケードにおける役割までを体系的に解説しました。
ビタミンKは単に「血を固める栄養素」ではなく、凝固因子をカルボキシル化することでCa²⁺を介した集積を可能にし、止血反応を成立させる基盤を担う分子です。
血液凝固は血小板反応と凝固カスケードが精密に連携した現象であり、その中核にビタミンK依存的な分子機構が存在します。これらの理解は、止血の仕組みを正しく捉えるだけでなく、ビタミンKの機能とその生理的意義を体系的に理解する上で不可欠です。
参考文献
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp. 280-285,
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp. 172
- Peter J. Kennelly, Kathleen M. Botham, Owen P. McGuinness, Victor W. Rodwell, P. Anthony Weil 著、清水孝雄、水島昇 監訳 (2024). イラストレイテッド ハーパー・生化学 原書32版. 丸善出版. pp. 633-650
- 五十嵐脩、江指隆年 編 (2011). ビタミン・ミネラルの科学. 朝倉書店. pp. 1–39
- John E. Hall 著、石川義弘、岡村康司、尾仲達史、河野憲二 総監訳、金子猛、北村義浩、藤乘嗣泰、松嶋成志 監訳 (2022). ガイトン生理学 原著第13版. エルゼビア・ジャパン株式会社. pp. 434-445, 820.
- Hammed, A., Matagrin, B., Spohn, G., Prouillac, C., Benoit, E., & Lattard, V. (2013). VKORC1L1, an enzyme rescuing the vitamin K 2,3-epoxide reductase activity in some extrahepatic tissues during anticoagulation therapy. Journal of Biological Chemistry, 288(40), 28733–28742. https://doi.org/10.1074/jbc.M113.457119
- Rishavy, M. A., & Berkner, K. L. (2012). Vitamin K oxygenation, glutamate carboxylation, and processivity: Defining the three critical facets of catalysis by the vitamin K-dependent carboxylase. In Advances in Nutrition (Vol. 3, Issue 2, pp. 135–148). https://doi.org/10.3945/an.111.001719
- Shen, G., Cui, W., Cao, Q., Gao, M., Liu, H., Su, G., Gross, M. L., & Li, W. (2021). The catalytic mechanism of vitamin K epoxide reduction in a cellular environment. Journal of Biological Chemistry, 296. https://doi.org/10.1074/jbc.RA120.015401
- Wishart, D. S. ほか (2024). The Natural Products Magnetic Resonance Database (NP-MRD). Nucleic Acids Research. https://np-mrd.org/natural_products/NP0337491
- de Souza, A. S., Ribeiro, R. C. B., Costa, D. C. S., Pauli, F. P., Pinho, D. R., de Moraes, M. G., de C. da Silva, F., da S.M. Forezi, L., & Ferreira, V. F. (2022). Menadione: a platform and a target to valuable compounds synthesis. In Beilstein Journal of Organic Chemistry (Vol. 18, pp. 381–419). Beilstein-Institut Zur Forderung der Chemischen Wissenschaften. https://doi.org/10.3762/bjoc.18.43
- Huang, M., Rigby, A. C., Morelli, X., Grant, M. A., Huang, G., Furiel, B., Seaton, B., & Furie, B. C. (2003). Structural basis of membrane binding by Gla domains of vitamin K-dependent proteins. Nature Structural Biology, 10(9), 751–756. https://doi.org/10.1038/nsb971
- Wang, J., Yu, C., Zhuang, J., Qi, W., Jiang, J., Liu, X., Zhao, W., Cao, Y., Wu, H., Qi, J., & Zhao, R. C. (2022). The role of phosphatidylserine on the membrane in immunity and blood coagulation. In Biomarker Research (Vol. 10, Issue 1). BioMed Central Ltd. https://doi.org/10.1186/s40364-021-00346-0
- Cristina Lazăr, A., Ilea, A., Moldovan, B., Ionel, A., Simona Pop, A., Păcurar, M., & Septimiu Câmpian, R. (n.d.). State of the art regarding anticoagulant and thrombolytic therapy in dental procedures. Rom J Morphol Embryol, 2019(2), 403–410. Retrieved http://www.rjme.ro/