ビタミンAは、外界からの光情報を受け取り、それを生体内のシグナルへと変換する重要な分子です。この機能はレーダーのように、微弱な光を検知し、それを増幅して伝達する仕組みにたとえることができます。光を受け取ると、ロドプシンの補欠分子族であるレチナール(ビタミンAの代謝物)が構造変化を起こし、シグナル伝達が開始されます。このシグナルは光受容器細胞内で増幅され、最終的に脳で処理されることで、私たちの行動や認識につながります。
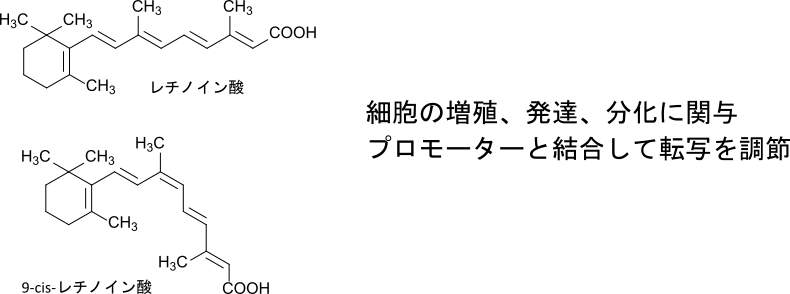
一方で、ビタミンAの代謝物であるレチノイン酸はホルモン様の作用を持ち、核内受容体と結合して遺伝子発現を調節します。特に9-cis-レチノイン酸を認識するRXRは、TR、RAR、VDR、PPAR、FXRなどの核内受容体とヘテロ二量体を形成し、それぞれのリガンドに応じて多様な生理機能を制御します。
本記事では、ビタミンAについて構造から吸収・輸送、さらに視覚の作用機序や核内受容体を介した遺伝子発現調節までを体系的に解説します。ビタミンAを起点として、視覚や遺伝子発現制御といった生体内の情報処理機構への理解を深めてください。
ビタミンA の構造とプロビタミンA
ビタミンAの構造と種類
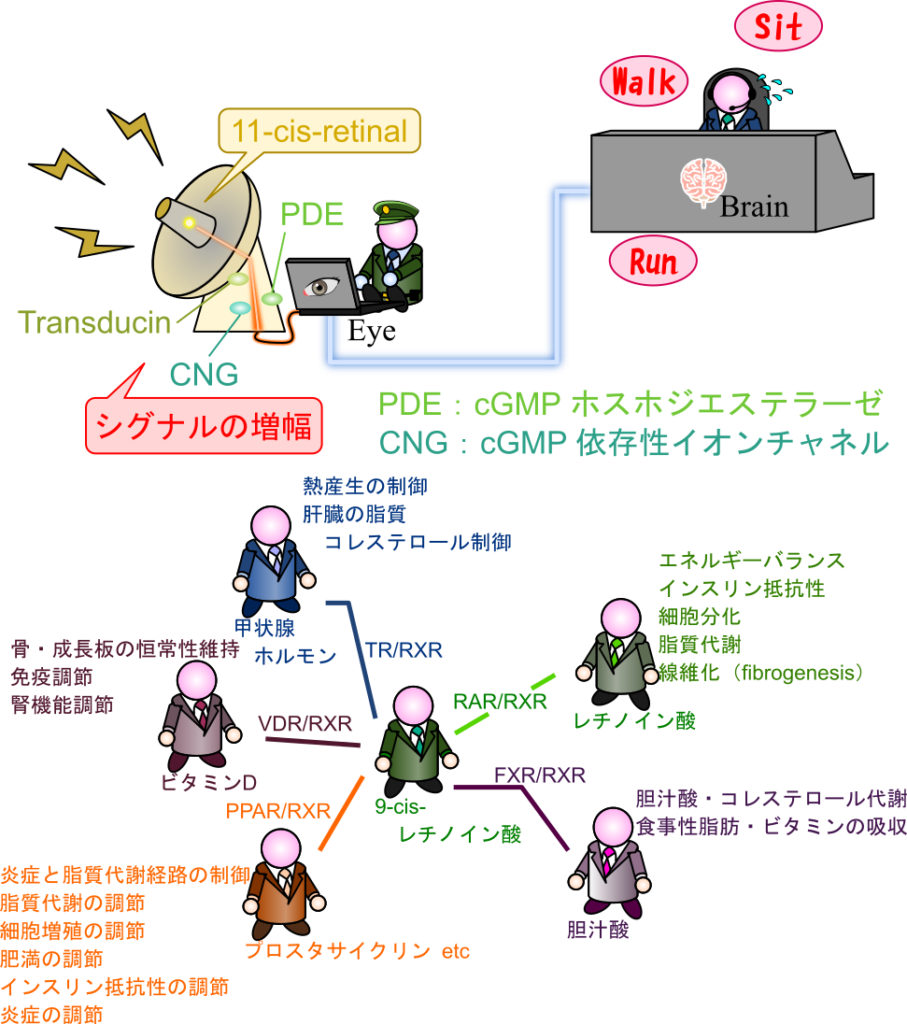
ビタミンAの化学名はレチノールと呼ばれ、成長促進、視覚の正常化、上皮細胞の正常化、生殖機能の維持、子宮内膜、卵子、精子の正常な機能、感染予防、血管の強化、気管支の粘膜正常化、免疫細胞の機能維持などに関与しています。レチノールはβ-ヨノン環を持つ、イソプレン単位が四つで構成されているテルペノイドで、代謝の過程で酸化されてレチナールやレチノイン酸に変換されます(図 1)。レチノールは一つ置きに二重結合が位置している構造(ポリエン)を持っており、この構造の π 電子が自由度を持っています。この特性は光を受け取ってシグナルを伝達するうえで重要な構造上の特徴です。また、レチノールが酸化されて生成されるレチノイン酸はある種のシグナル伝達に重要です。レチノイン酸にはすべての二重結合が trans 型を取る all-trans-レチノイン酸と 9 位の二重結合が cis 型を取る 9-cis-レチノイン酸があります。これらのレチノイン酸は異なるレセプターに認識され、異なるシグナルを伝達して遺伝子発現を調節します。
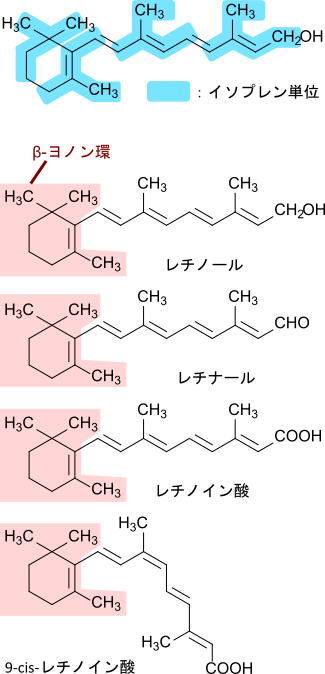
プロビタミンA(カロテノイド)の構造とレチノールへの変換
プロビタミンAにはαカロテンや βカロテン、クリプトキサンチンなどが知られています(図 2)。βカロテンはレチノール二分子が縮合したような構造をしており、体内で解離することでレチノールに変換されます(図 3)。
βカロテンの開裂は酸素分子が 15 位と 15’ 位の間に付加されることで始まります。生成された βカロテン-15,15’-ペルオキシドは開裂して二分子のレチナールを生成します。レチナールは NADPH を消費してホルミル基を還元し、レチノールを生成します。このようにカロテノイドは体内で代謝を受けることでレチノールへと変換されるのです。理論的には β カロテン1分子の開裂によりレチノールは2分子が生成する計算となりますが、このうち体内で利用されるのは1分子だけですので、栄養学的には β カロテン1分子からレチノールは1分子が生成されることになります。
一般に βカロテンの利用率は脂肪の摂取量や食物の細胞膜の硬さなどに左右されますが、一般に 1/6 程度とされています。このことを踏まえてレチノール1 μgに相当する βカロテンは 12 μg 程度と想定されています。一方でαカロテンやクリプトキサンチンのように分子内にヨノン環を一つしか持たないカロテノイドの場合、24 μg がレチノール 1 μg に相当するとされています。

ビタミンA・プロビタミンAの吸収
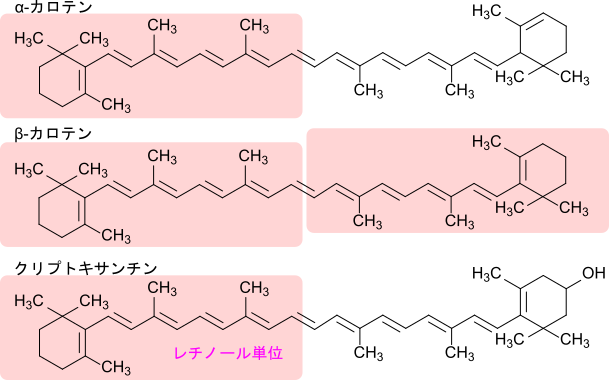
ビタミンAとプロビタミンAの吸収と輸送を図 4に示します。レチノールは食品中ではレチニルエステルとして存在している場合があります。この場合はリパーゼの作用により加水分解されて、レチノールが遊離します。遊離されたレチノールは胆汁酸の作用によりミセルに取り込まれます。カロテノイドも脂溶性であるためミセルに取り込まれます。これらの分子はミセルを介して粘膜に取り込まれ、カロテノイドはこの粘膜中で前述のように開裂してレチナールを生成し、さらに還元されてレチノールへ変換されます。生成または吸収されたレチノールはレチニルエステルに変換されてキロミクロン中に取り込まれ、血中に放出されます。キロミクロンはこれらのレチニルエステルやカロテノイドを肝臓に輸送します。カロテノイドのレチノールへの変換は主に小腸粘膜内で行われますが、肝臓内でも一部行われます。一方で、レチニルエステルは加水分解されてレチノールへ変換されます。これらのレチノールはレチノール結合タンパク質(retinol binding protein; RBP)やアルブミンと結合して血中を輸送されます。末梢細胞に運搬されたレチノールは細胞内で細胞内レチノール結合タンパク質(cellular retinol binding protein; CRBP)と結合したり、レチノイン酸に変換されて様々な機能に利用されます。一方で、一部のレチノールは再エステル化されて、細胞内に貯蔵され、必要に応じて加水分解されて利用されます。レチノイン酸などはシグナル物質として核内レセプターと結合して一部の遺伝子発現を誘導します。
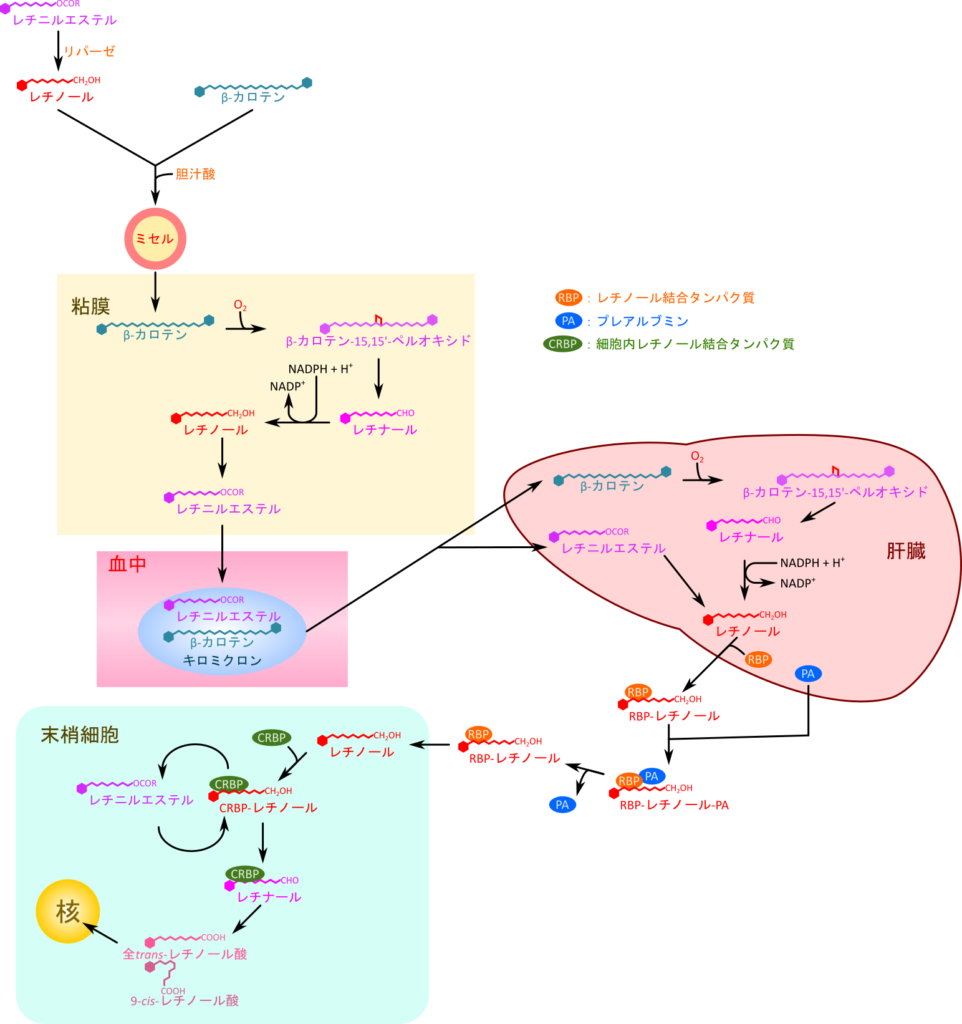
視覚とビタミンA
ビタミンAの最も重要な機能の一つは視覚の正常化です。この項目では視覚の仕組みを確認したのちに、ビタミンAが視覚にどのように貢献しているのかを解説します。
光受容器細胞と光受容体分子
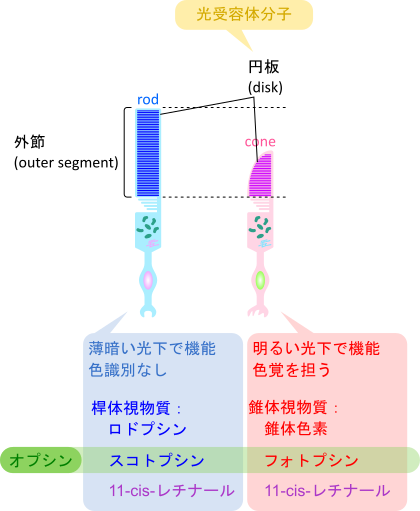
光受容器細胞には形態的な特徴から桿体細胞(rod cell)と錐体細胞(cone cell)に分けられます(図 5)。桿体細胞は薄暗い光の下で機能して感度が高く色の識別はしません。人の網膜には桿体細胞が1億個程度含まれています。一方で錐体細胞は明るい光の下で機能する光受容器細胞で三種類の錐体細胞が存在しています。これらの錐体細胞の吸収極大は以下の三種類が知られています。
- 約420 nm(S錐体)
- 約530 nm(M錐体)
- 約560 nm(L錐体)
これらの錐体はそれぞれ異なる光受容体分子を持ちますが、異なる光受容体分子の存在が色の識別に関与します。
光受容体分子はオプシン(opsin)と呼ばれるタンパク質部分と補欠分子族の11-cis-レチナールから成り立っています。桿体細胞では光受容体分子はロドプシン(rhodopsin)ですが、ロドプシンはスコトプシン(scotopsin)と補欠分子族の11-cis-レチナールから成り立っています(図 7)。11-cis-レチナールはオプシンのリシン残基に結合してシッフ塩基を形成しており、吸収極大がより長波長側にある要因となっています(プロトン化されていない状態では吸収極大は 380 nm 付近にありますが、プロトン化されてシッフ塩基を形成すると440 nm 以上にシフトします;図 6)。また、11-cis-レチナールは二重結合を多数持つポリエンであり、ポリエンの π 電子は非局在化しているためにポリエン全体に広がっている配置をとります。連続した二重結合の配置のため、π 電子が励起しやすい状態となっており、この特性が光を吸収することに貢献します。11-cis-レチナールのポリエンはかなり長い構造を持っており吸収極大がより長波長側にある要因となります(ポリエンは長ければ長いほど電子の励起に要するエネルギーが減少するため、吸収極大が長波長側に移行します)。後述しますが11-cis-レチナールは周囲のアミノ酸配列によっても影響を受けて吸収極大がシフトします。つまり11-cis-レチナールは
- シッフ塩基の形成
- 長いポリエン構造
- 周囲のアミノ酸配列
の三つの要素のために吸収極大が 500 nm 付近にあります。
このように 11-cis-レチナールは良質な光受容体としてセンサーの役割を担うことが可能です。一方で、錐体細胞は前述のようにS錐体、M錐体、L錐体の三種類があります。これらの細胞の光受容体分子はロドプシンと類似した光受容体分子、錐体色素(cone pigment)によって担われていますが、スコトプシンと相同な(同一祖先から派生した)分子であるフォトプシン(photopsin)と 11-cis-レチナールから成り立っています。このフォトプシン(ヒトではSオプシン、Mオプシン、Lオプシンの三種類があり、種類の数は生物種によって異なります)の配列の違いが吸収極大の差を生み出しています。
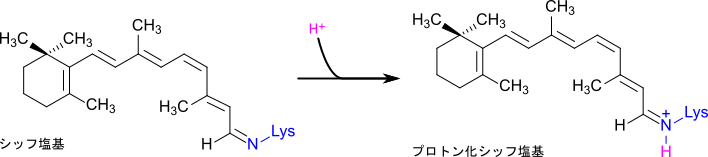
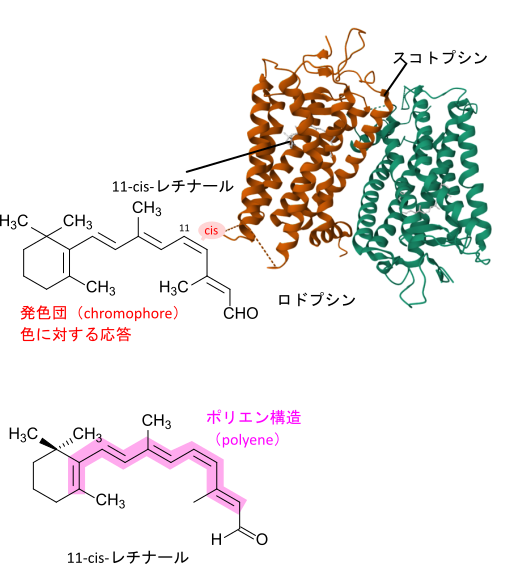
桿体細胞の過分極と脱分極
脱分極と過分極の誘導
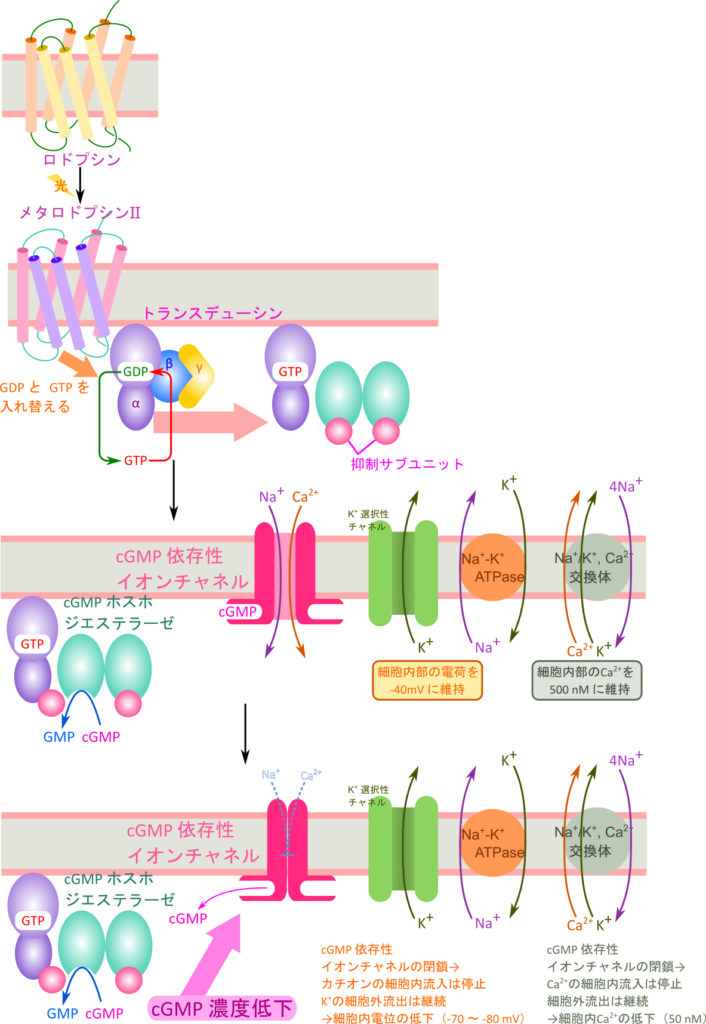
桿体細胞が光の刺激を受けていない条件下(暗条件下)では cGMP 依存性イオンチャネルを介してNa+を取り込む一方で、Na+-K+ ATPase がATP を消費して K+ と交換にNa+ を細胞外にくみ出します。この時取り込んだ K+ は K+ 選択性チャネルを通じて細胞外へ拡散していきます。このNa+ と K+ の取り込みとくみ出しのバランスによって桿体細胞内の電位が ー40 mV 程度に保たれます(脱分極;depolarization)。
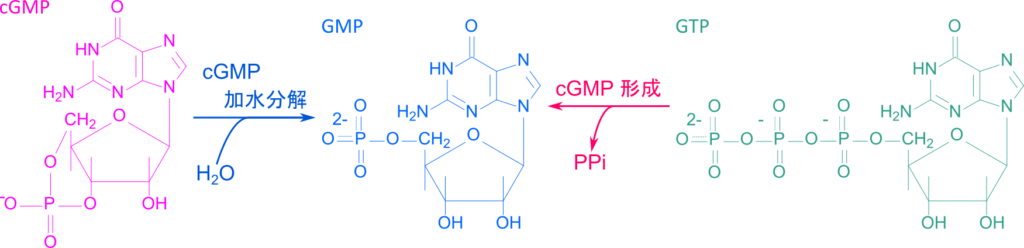
桿体細胞が光の刺激を受け取るとロドプシンが構造変化を起こしてメタロドプシンⅡへ変換されます。この時、ロドプシンのレチナールが起こす構造変化によって、ロドプシン近傍のトランスデューシンが活性化されます。トランスデューシンは α、β、γ サブユニットから構成されており、αサブユニットは不活性型の場合、GDP と複合体を形成しています。活性化されたロドプシンは α サブユニットの GDP を GTP に交換します。GTP 型となった α サブユニットは βγ サブユニットから解離して cGMP ホスホジエステラーゼと結合し、cGMP ホスホジエステラーゼの活性を抑制している抑制サブユニットを外します。この作用により cGMP ホスホジエステラーゼは cGMP の 5’ のリン酸基と 3’ の水酸基間を加水分解して解離させ、5’-GMP に変換します(図 10)。この結果引き起こされた細胞内 cGMP 濃度の低下は cGMP 依存性イオンチャネルの閉塞を誘導し、Na+ の流入を停止させます。一方で、Na+-K+ ATPase によるNa+ のくみ出しは継続しているため(なお、K+ の流入と流出は継続しています)細胞内電位は低下し、-70~-80 mV まで低下します。この状態を過分極(hyperpolarization)と呼び、ニューロンシグナル伝達の起点となります(図 8)。過分極カスケードを経ることによりわずかな光のシグナルでも増幅され、十分に大きなシグナルとして伝達が可能となります。
一方で、cGMP 依存性イオンチャネルでは Ca2+ も流入していますが、Ca2+ はNa+/Ca2+-K+ 交換体を介してくみ出されます。Ca2+ 一分子は K+ とともに4分子のNa+ の取り込みと交換でくみ出されます。この作用により、暗条件下では Ca2+ は 500nM 程度に維持されています。このことは後述する脱分極において重要となります。
桿体細胞の脱分極
視覚系は非常に素早い応答が可能ですが、このような反応が達成されるためには、誘導されたシグナルを素早く終了させて暗条件の状態に戻さなければなりません。この状態は脱分極と呼ばれています。再脱分極の過程は三つのメカニズムにより進行します(図 9)。
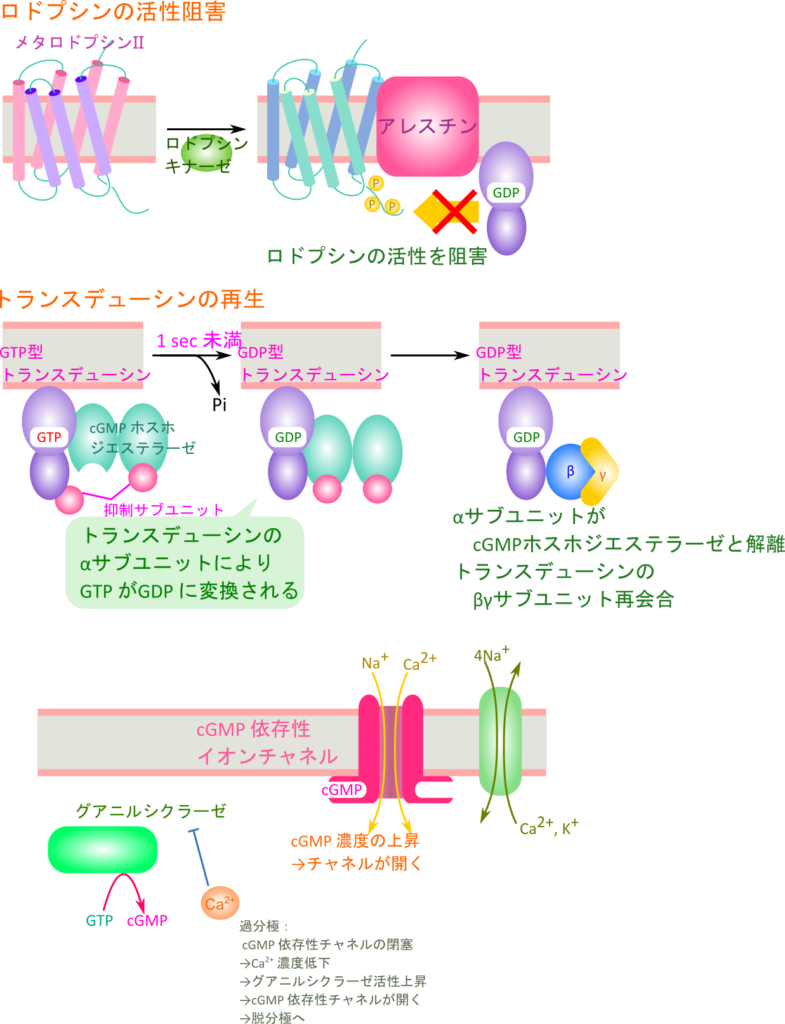
- ロドプシンの活性阻害
- トランスデューシンのαサブユニットの不活性化とトランスデューシンの再生
- cGMP 濃度の回復
ロドプシンの活性阻害では、活性化されたロドプシンはロドプシンキナーゼの作用により、セリンやトレオニンをリン酸化され、ロドプシンの阻害因子であるアレスチンがリン酸化されたロドプシンに結合して、ロドプシンとトランスデューシンの相互作用を阻害します。
次にトランスデューシンの α サブユニットの不活性化とトランスデューシンの再生では、トランスデューシンの α サブユニットは cGMP ホスホジエステラーゼと結合した後、1秒未満に GTP が加水分解されて GDP へ変換されます。この結果、α サブユニットは不活性な状態(GDP 型)へ移行し、cGMP ホスホジエステラーゼから解離して βγ サブユニットと再会合します。
最後に cGMP 濃度の回復では、加水分解されて減少した cGMP をグアニル酸シクラーゼが GTP を cGMP に変換することで回復させます。
グアニル酸シクラーゼは Ca2+ によって著しく阻害を受けます。暗条件下ではCa2+ 濃度は 500 nM 程度に維持されています。このためグアニル酸シクラーゼ活性は強く阻害されています。一方で過分極により細胞内 Ca2+ 濃度は 50 nM 程度にまで低下します。この結果十分に低い Ca2+ 濃度となりグアニル酸シクラーゼの Ca2+ による阻害が外れ、cGMP 濃度は回復します。この結果 cGMP 依存性イオンチャネルは再び開くこととなり、桿体細胞は最初の状態へ戻ります(図 9)。
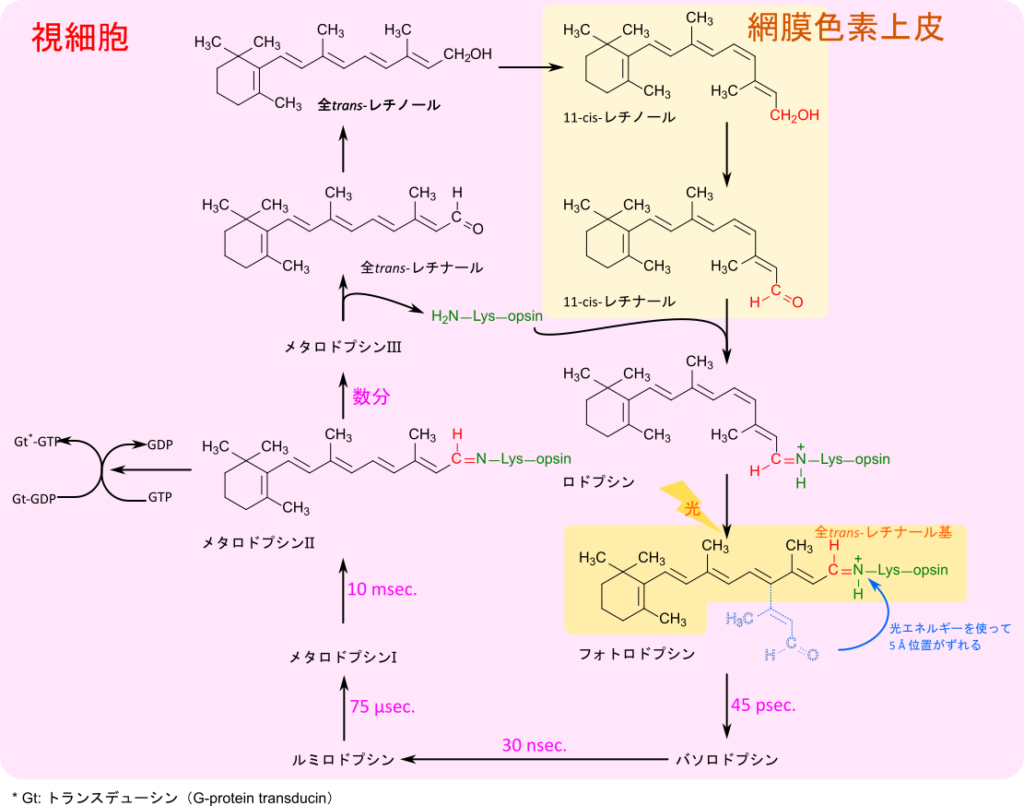
視覚回路におけるレチナールの変化
ロドプシンが光を受け取ると、ロドプシンは構造変化を起こしてトランスデューシンの活性化を誘導したのち、再生され、暗条件下のロドプシンが再生されます。光の刺激により、ロドプシン中の11-cis-レチナールが異性化して全 trans レチナールに変化します。この変化によりレチノール分子は折れ曲がった構造から直鎖状の構造に変化し、レチナール分子は約 5 Å程度移動します。このようにして生成されたフォトロドプシンはその後、バソロドプシン、ルミロドプシン、メタロドプシンⅠを経てメタロドプシンⅡに変換されます。メタロドプシンⅡはトランスデューシンを活性化したのち、メタロドプシンⅢを経てレチナールとオプシンが解離します。遊離したレチナールは還元されてレチノールへ変換されます。レチノールは網膜色素上皮(retinal pigment epithelium; RPE)へ輸送されて異性化を受けて 11-cis-レチノールとなります。11-cis-レチノールは酸化されて 11-cis-レチナールとなり、オプシンと複合体を形成することでロドプシンとなります。この過程は視覚回路(visual cycle)と呼ばれています(図 11)。
シグナル伝達物質としてのビタミンA
レチノールから誘導されるレチノイン酸や 9-cis-レチノイン酸はシグナル伝達物質として機能し、ある種の遺伝子発現を誘導する機能を担います(図 12)。
レチノールの細胞内輸送と貯蔵、レチノイン酸の生合成
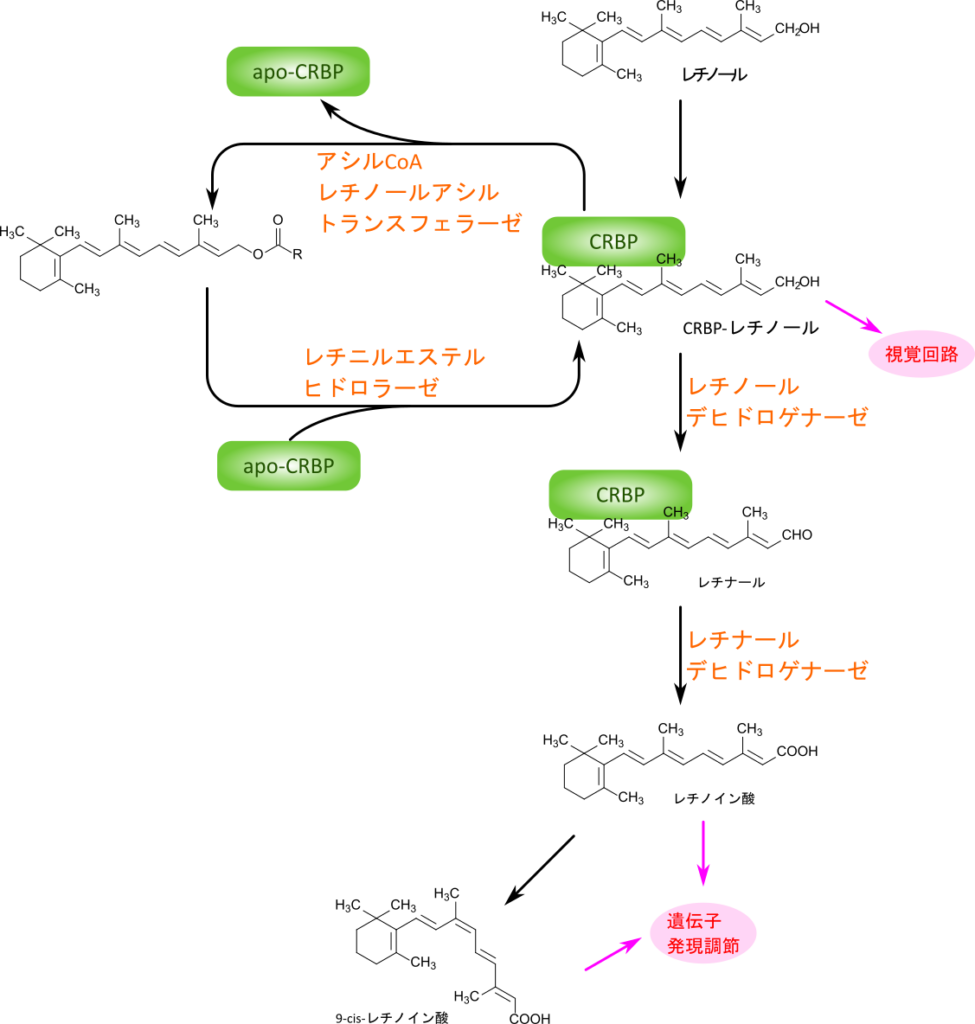
末梢細胞に輸送されたレチノールは細胞に取り込まれると細胞内レチノール結合タンパク質(cellular retinol binding protein; CRBP)と結合します。レチノールはアシル CoA レチノールアシルトランスフェラーゼの作用によりレチノールエステルに変換されます。レチノールエステルは細胞内におけるレチノールの貯蔵形態です。レチノールエステルはレチニルエステルヒドロラーゼによって加水分解を受けてレチノールに変換され、利用されます。レチノールは前述の通り視覚回路に利用されますが、一部はレチノールデヒドロゲナーゼ、レチナールデヒドロゲナーゼの作用により酸化されていき、レチノイン酸に変換されます。このレチノイン酸自身も遺伝子発現調節を担います。一方で、レチノイン酸がさらに異性化を受けると 9-cis-レチノイン酸が生成されます。この9-cis-レチノイン酸も遺伝子発現を誘導します(図 13)。
レチノイン酸によるシグナル伝達と核内レセプタースーパーファミリー
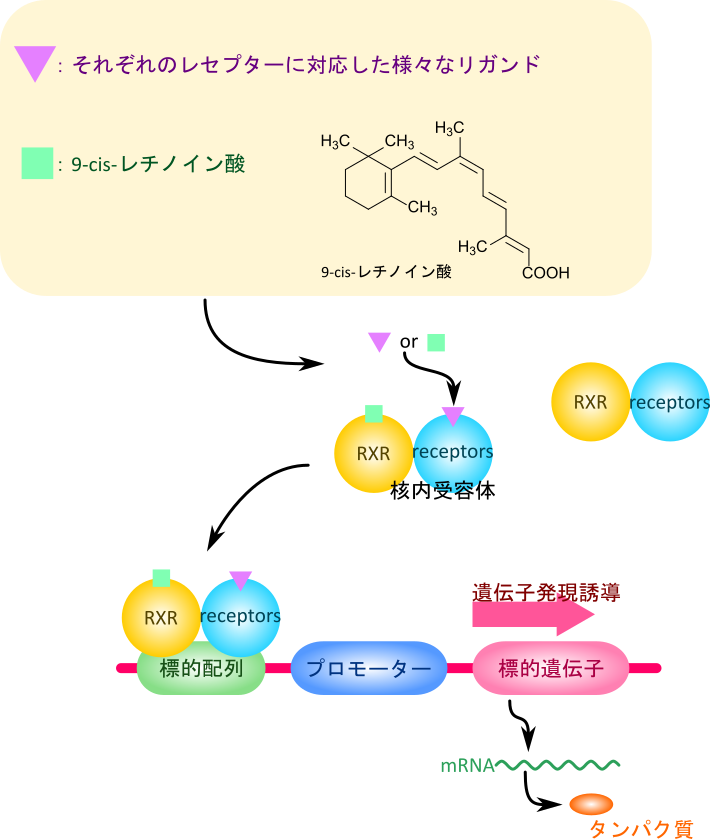
レチノイン酸や 9-cis-レチノイン酸は核内レセプターと結合してさまざまなシグナル伝達に関与します。9-cis-レチノイン酸のレセプターであるレチノイン酸 X レセプター(Retinoic acid X receptor; RXR)は他のレセプターとヘテロダイマーを形成しています。RXR やレチノイン酸のレセプターであるレチノイン酸レセプター(Retinoic Acid Receptor; RAR)は核内レセプタースーパーファミリーに属しています。RXR は RAR を含む核内レセプターと会合して二量体(ヘテロ二量体)を形成し、様々なシグナルを媒介しています(表 1)。これらの核内レセプターにリガンドが結合すると、核内レセプターはゲノム上の標的エンハンサー領域に結合し、標的遺伝子の発現を調節します(図14)。RXR/RAR、RXR/VDR などのヘテロ二量体の結合する標的エンハンサー領域は標的遺伝子の発現をリガンド依存的に活性化させる機能を発揮するので、リガンド応答配列(Ligand Response Element; LRE)と呼ばれています。この配列は RGKTCA (ただし、R: A or G、K: G or T)を基本とした2個のモチーフの繰り返し(Direct Repeat; DR)配列から構成されています。このモチーフ間のスペース塩基数によって DR 1~5 に分類されています。DR 1(2配列間の塩基数が1 bp)、DR2(2配列間の塩基数が2 bp)、DR5(2配列間の塩基数が5 bp)についてはレチノイン酸応答配列(Retinoic Acid Response Element; RARE)と呼ばれています。一方でDR3(2配列間の塩基数が3 bp)の場合はビタミンD応答配列(Vitamin D Response Element; VDRE)、DR4(2配列間の塩基数が4 bp)の場合は甲状腺ホルモン応答性配列(Thyroid Hormone Response Element; TRE)として機能します。
| 核内受容体 | 内因性/合成リガンド | 作用(生理機能) |
| TR (Thyroid hormone Receptor) | thyroxine triiodothyronine | 熱産生(thermogenesis)の制御(TRα) 肝臓の脂質/コレステロール制御(TRβ) |
| RAR (Retinoic acid Receptor) | レチノイン酸 | エネルギーバランス インスリン抵抗性 細胞分化 脂質代謝 線維化(fibrogenesis) |
| PPAR(Peroxisome Proliferator-Activated Receptor) | 脂肪酸 エイコサノイド リン脂質 プロスタサイクリン(PGI2) プロスタグランジンJ2(PGJ2) リノール酸 酸化LDL | 炎症と脂質代謝経路の制御 脂質代謝の調節 細胞増殖の調節 肥満の調節 インスリン抵抗性の調節 炎症の調節 |
| LXR(Liver X Receptor) | オキシステロール | 肝脂肪生成の制御 逆コレステロール輸送 抗炎症 |
| FXR(Farnesoid X receptor) | 胆汁酸 | 胆汁酸・コレステロール代謝 食事性脂肪・ビタミンの吸収 |
| VDR(Vitamin D Receptor) | 1,25-ジヒドロキシビタミンD3 カルシトリオール | 骨・成長板の恒常性維持 免疫調節 腎機能調節 |
| PXR(Pregnane X Receptor) | 内因性化学物質 (プレグナン、ステロイド、胆汁酸) 臨床薬、環境汚染物質 | 解毒 代謝の調節 炎症の調節 抗酸化ストレス |
| CAR(Constitutive Androstane Receptor) | 異物 内因性物質 | 薬物代謝 エネルギー恒常性維持 がん進展(種間差あり) 胆汁酸恒常性維持 糖・脂質恒常性維持 |
| RXR(Retinoid X Receptor) | 9-cis-レチノイン酸 脂肪酸 | 脂質・糖代謝 |
| COUP-TF(Chick Ovalbumin Upstream Promoter-Transcription Factor) | 内因性リガンド(不明) | 胚発生 中枢神経発生 細胞増殖と腫瘍形成 脂肪細胞分化 脂質恒常性維持 エネルギー消費 |
| Nur77 / Nurr1 / NOR1 | 内因性リガンド(不明) | 増殖 アポトーシス 細胞ストレス DNA修復 内分泌の調節 神経シグナル 造血 免疫・代謝過程 |
| Li, F., Chen, Q., Dai, Y., & Lu, L. (2025). Nuclear receptors as therapeutic targets in metabolic and cardiovascular disorders. In iScience (Vol. 28, Issue 12). Elsevier Inc. https://doi.org/10.1016/j.isci.2025.114042 | ||
核内レセプターによる遺伝子発現調節のメカニズム
RAR/RXR ヘテロ二量体のような核内レセプターがリガンドと結合すると核内レセプターの構造変化を引き起こして、転写共役因子複合体と核内レセプター/リガンド複合体の相互作用が惹起されます。転写共役因子複合体は ATP 依存性染色体構造調節因子(ATP dependent remodeling complex)によりヌクレオソーム構造を変化させるとともに、コアクチベーター複合体(CBP/p300、SRC-1/TIF2など)のHAT活性によりヒストンがアセチル化されてクロマチン構造が緩み、遺伝子転写に必要な種々の因子がアクセスできるようになります。逆に、コリプレッサー複合体(NCoR、SMRTなど)のHDAC活性により脱アセチル化されると遺伝子発現が抑制されます(図15)。
なお、これらのレセプターとリガンドの関係は現在も研究が進められている領域であり、新たにリガンドが発見されたり、リガンドが未同定のもの(orphan receptor)も含まれています。
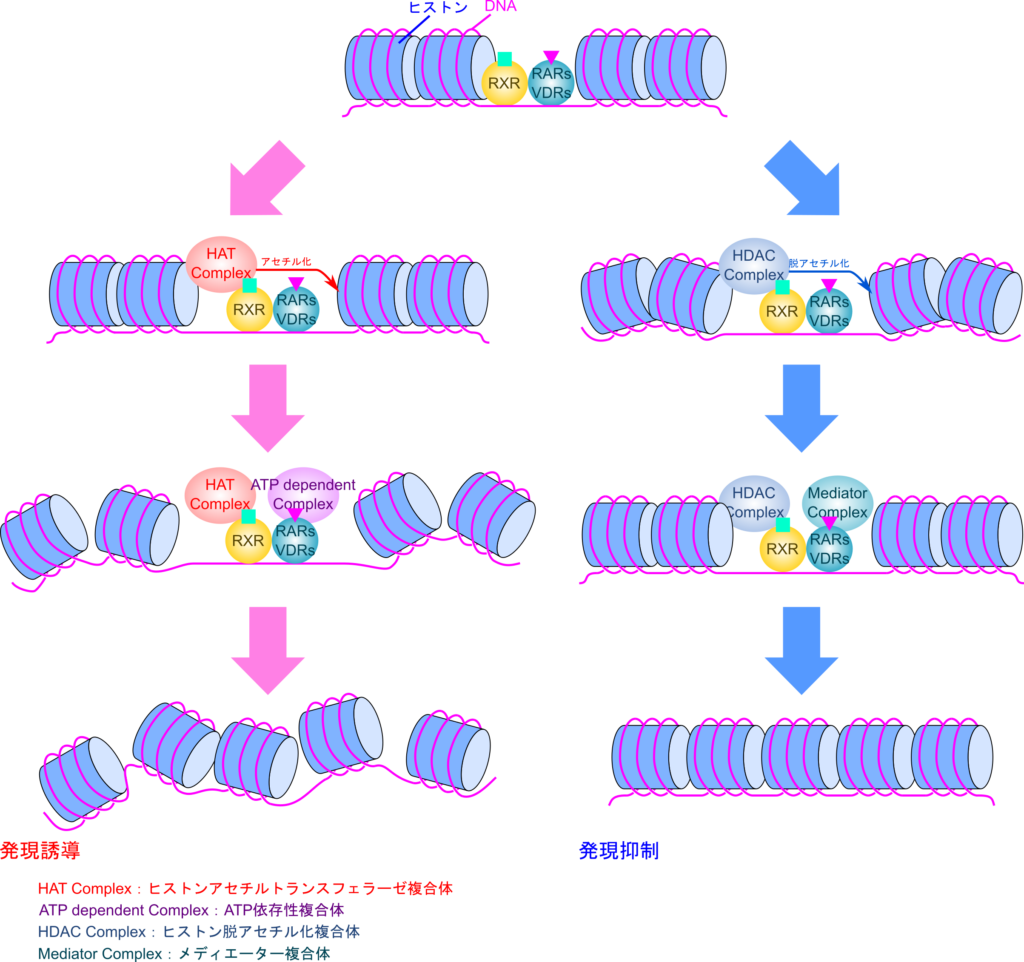
図 15. 核内レセプターによる遺伝子発現調節機構
練習問題
この記事では、ビタミンAの構造、吸収・輸送から生理的機能に至るまでを体系的に解説しました。ビタミンAは視覚情報の受容と伝達に関与するだけでなく、レチノイン酸を介した遺伝子発現調節においても、核内受容体と協調して機能する重要な分子です。本記事ではこれらの機構を統合的に捉え、視覚の作用機序や核内レセプタースーパーファミリーの理解にもつながるように解説しました。ビタミンAを起点として、視覚や遺伝子発現制御といった生体内の情報処理機構への理解を深めていただければ幸いです。
参考文献
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp. 391-415, 416-458, 459- 484, 485-522, 633-662, 665-693, 597-632, 888-906
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp. 164-195, 216-241, 293-313, 440-476, 477-513
- Peter J. Kennelly, Kathleen M. Botham, Owen P. McGuinness, Victor W. Rodwell, P. Anthony Weil 著、清水孝雄、水島昇 監訳 (2024). イラストレイテッド ハーパー・生化学 原書32版. 丸善出版. pp. 633-350
- 五十嵐脩、江指隆年 編 (2011). ビタミン・ミネラルの科学. 朝倉書店. pp. 1–39
- John E. Hall 著、石川義弘、岡村康司、尾仲達史、河野憲二 総監訳、金子猛、北村義浩、藤乘嗣泰、松嶋成志 監訳 (2022). ガイトン生理学 原著第13版. エルゼビア・ジャパン株式会社. pp. 579-592
- Choi, E. H., Daruwalla, A., Suh, S., Leinonen, H., & Palczewski, K. (2021). Retinoids in the visual cycle: role of the retinal G protein-coupled receptor. Journal of Lipid Research, 62, 100040. https://doi.org/10.1194/jlr.TR120000850
- 河村悟. (1999). 視覚と受容体の順応・適応機構. 生産と技術, 51(1), 17–21.
- Li, F., Chen, Q., Dai, Y., & Lu, L. (2025). Nuclear receptors as therapeutic targets in metabolic and cardiovascular disorders. In iScience (Vol. 28, Issue 12). Elsevier Inc. https://doi.org/10.1016/j.isci.2025.114042