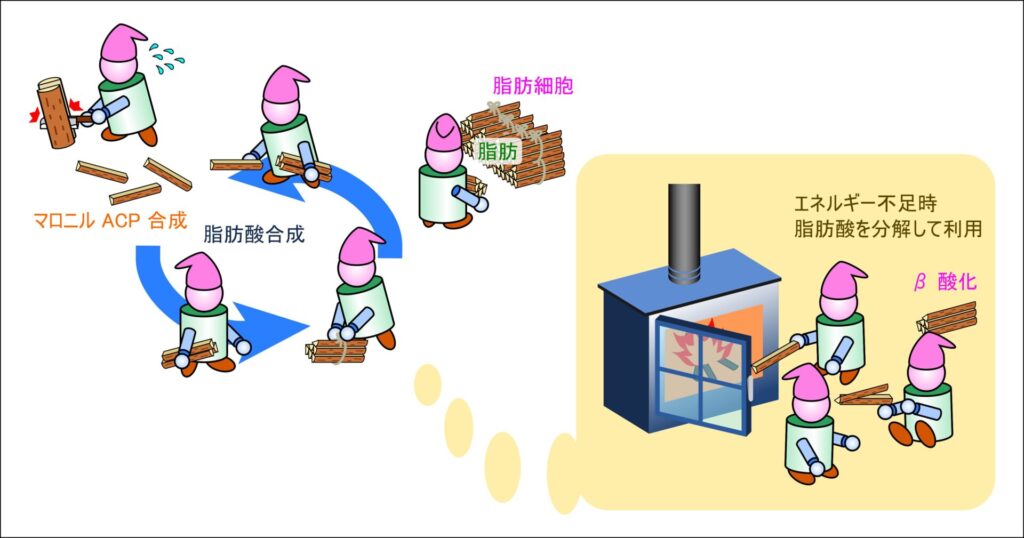
脂肪酸合成は薪が不足する冬に向けて薪を保管する作業に似ています。賢い先人たちは冬場の薪が取れにくくなる季節に向けてこれら薪が豊富に確保できる夏場や秋に薪を蓄えていました。脂肪酸合成も同様で、エネルギーが豊富に入手可能な時に薪(マロニル ACP)をまとめて薪の束(脂肪)として蓄えておきます。こうすることでエネルギー不足時に脂肪を分解することでエネルギーを入手することが可能となります。ところで、脂肪酸合成は分解の逆反応ではありません。β 酸化との相違点から、マロニルCoA・NADPH・ACPが関与する脂肪酸シンターゼの2炭素伸長、脂肪酸シンターゼの構造、化学量論までを図解付きで整理しています。具体的なイメージをつかみながら、学習・試験・研究の基礎固めに最適な記事となっています。ぜひこの記事を使って脂肪酸合成の理解を深めてください。
Contents
脂肪酸生合成経路と分解経路の相違点
脂肪酸の生合成は、脂肪酸の酸化(分解)の単純な逆反応ではありません。一見すると中間体が共通しているため逆反応のように見えますが、実際には多くの相違点をもつ独立した代謝経路です。具体的な反応過程をみる前に、両者の違いを整理してみましょう(表1)。
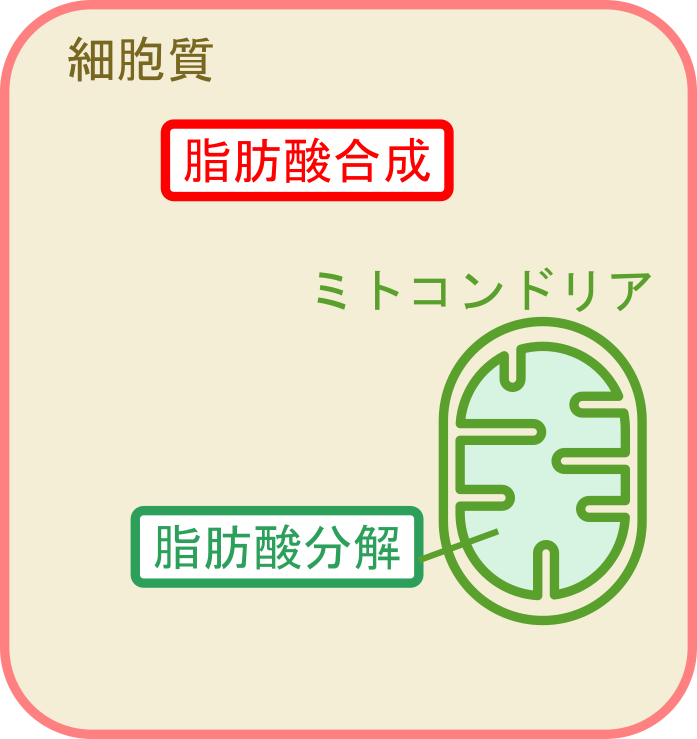
脂肪酸の生合成と分解の大きな相違点の一つは反応が起こる場所です。脂肪酸分解は主にミトコンドリアのマトリックス内で行われますが、脂肪酸合成は細胞質で行われます(図1)。この反応場所の違いは基質の輸送で重要となるので覚えておいてください。
次に、脂肪酸のキャリアとなる分子が異なります。脂肪酸の生合成と分解では、脂肪酸が酵素と相互作用しやすいように、脂肪酸と結合するキャリアが関与します。脂肪酸の分解では CoA がキャリアとして機能し、CoA の SH 基を介して脂肪酸と共有結合します。一方で、脂肪酸の生合成では、ACP がキャリアとして機能し、ACP の SH 基を介して脂肪酸と共有結合します。反応を触媒する酵素も異なります(図2)。
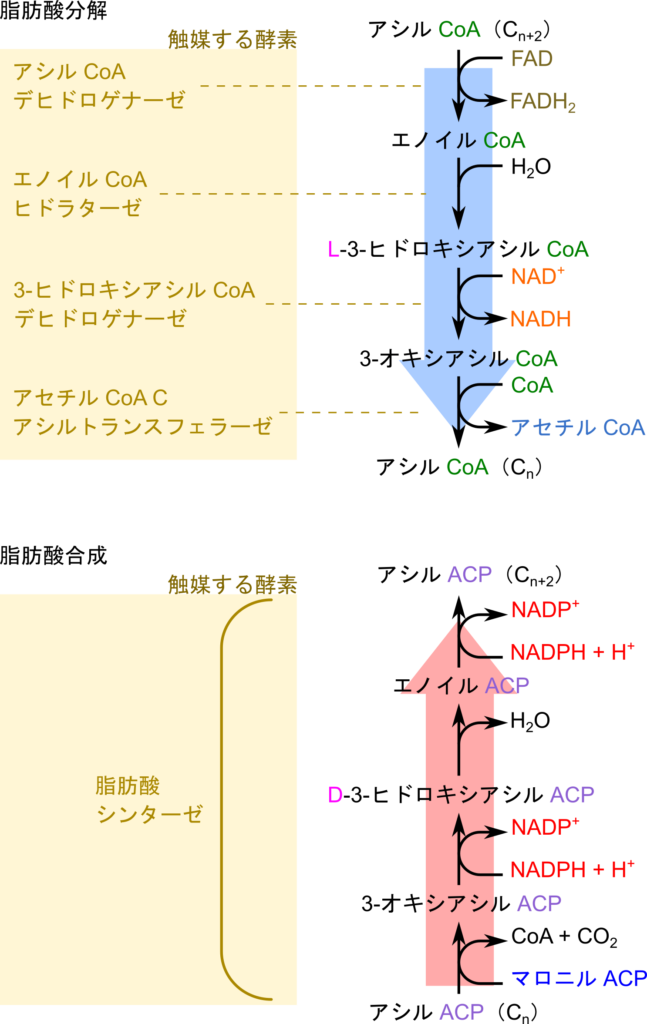
脂肪酸の分解ではアシル CoA デヒドロゲナーゼなど種々の酵素が反応を担当しますが、脂肪酸の生合成では脂肪酸シンターゼという大きな酵素が反応を触媒します(図2)。
脂肪酸を分解または合成する単位はいずれの経路もアセチル CoA であり、炭素数で2つずつですが、脂肪酸の生合成ではアセチル CoA を一度カルボキシル化してマロニル CoA とし、マロニル CoA の脱炭酸で発生するエネルギーを利用して反応を進めます。ですので、脂肪酸生合成の反応単位は実質、マロニル CoA です(図2)。
反応に関与する補酵素も異なります。脂肪酸の分解では酸化に NAD+ や FAD を利用しますが、脂肪酸の生合成ではNADPH を利用します(図2)。脂肪酸の生合成では生合成に関与する補酵素である NADPH が関与します。一方、脂肪酸の分解がエネルギーの取り出しが主たる目的であるために酸化的リン酸化でエネルギーに変換可能な NAD+ や FAD の方が都合が良いと考えると理解しやすいでしょう。
このように、脂肪酸の生合成は分解経路の単純な逆反応反応ではなく、異なる代謝経路なのです。
| 脂肪酸合成 | 脂肪酸分解 |
|---|---|
| 反応の場所:細胞質 | 反応の場所:ミトコンドリアのマトリックス |
| アシルキャリア―タンパク質 (acyl carrier protein; ACP)のSH 基に結合 | 補酵素 A(CoA)のSH基に結合 |
| 脂肪酸合成酵素(fatty acid synthase ;脂肪酸シンターゼ)により触媒 | いくつかの酵素により触媒 |
| アセチル CoA 由来炭素が二つずつ (実際にはマロニル ACP)が連続的に付加 CO2 の放出により駆動 | アセチルCoA 単位が遊離 |
| 還元に関与する補酵素は NADPH | 酸化に関与する補酵素は NAD+ と FAD |
脂肪酸合成と分解に関与するキャリア
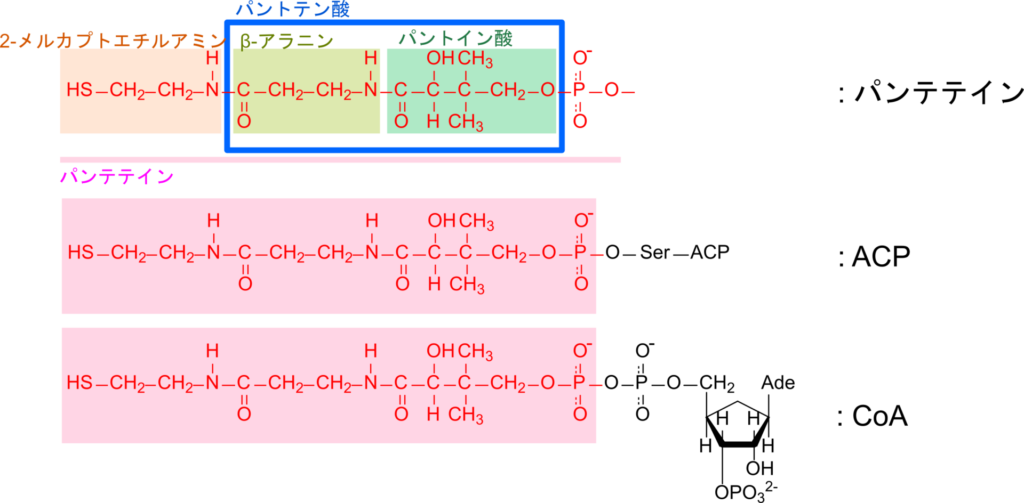
脂肪酸の生合成や分解には酵素が脂肪酸に関与しやすくなるようにキャリア分子が結合します。生合成と分解経路ではそれぞれ、アシルキャリアータンパク質(Acyl carrier protein;ACP)と補酵素A(Coenzyme A;CoA)という異なるキャリアが関与します。両者はパンテテイン部分(=パントテン酸+2-メルカプトエチルアミン)を共通に持っています。2-メルカプトエチルアミンにはチオール基が含まれますが、このチオール基は脂肪酸のカルボキシル基とチオエステル結合を形成して脂肪酸と結合するために利用されます。
一方で CoA はパンテテインと AMP で構成される遊離小分子であり、脂肪酸を活性化しますが、ACP ではセリン残基を介してパンテテインが酵素と結合し、脂肪酸を脂肪酸シンターゼに固定する役割を担います。
脂肪酸合成経路
脂肪酸合成の概要
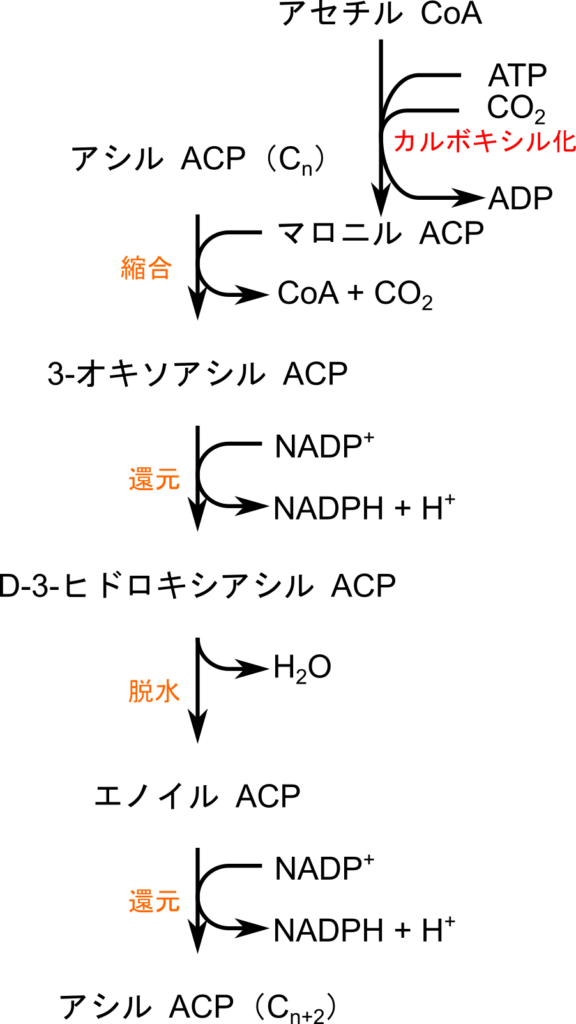
脂肪酸合成は脂肪酸シンターゼによって触媒されます。通常、脂肪酸合成は C16 の飽和脂肪酸であるパルミチン酸を生成します。さらに長い脂肪酸や二重結合を含む不飽和脂肪酸は脂肪酸シンターゼによる合成とは異なる機構により行われます。ここでは、基本となる脂肪酸シンターゼによる脂肪酸合成について見ていきましょう。
脂肪酸合成の伸長単位はマロニル ACP です。マロニル ACP はアセチル CoA に炭酸を付加することでマロニル CoA を介して生成されます。この時 ATP が消費されることからわかるように、マロニル ACP が脱炭酸する際にはエネルギーを生じます。このエネルギーはアシル ACP とマロニル ACP の縮合に利用されます。脂肪酸の伸長反応は以下の4段階で進みます。
- アシル ACP とマロニル ACP の縮合反応
- 3-オキソアシル ACP の還元反応
- D-3-ヒドロキシアシル ACP の脱水反応
- エノイル ACP の還元反応
この4段階の反応はすべて脂肪酸シンターゼにより触媒されます。タンパク質にはドメイン構造という部分構造があります。多くのタンパク質はこのドメイン構造の組み合わせにより実に多様な機能を発揮します。脂肪酸シンターゼには多くのドメインが含まれており、この部分構造それぞれが各反応を触媒しています。以下の説明ではこのドメイン名が出てきますが、脂肪酸合成を触媒する酵素は ACP も含めて脂肪酸シンターゼですので、これらのドメイン名は酵素名ではないので注意してください。なお、この記事ではドメイン名であることを明確にするために「~ドメイン」というように呼称することにします。
マロニル CoA の生成
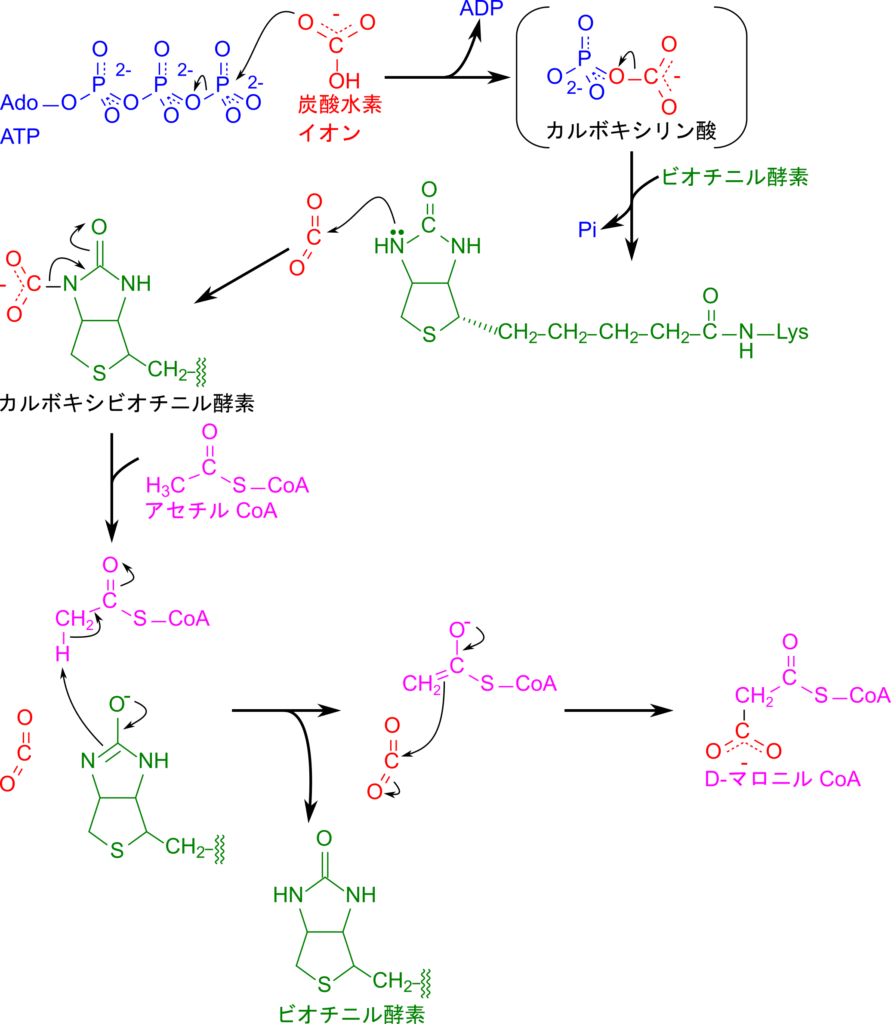
マロニル CoA はアセチル CoA をカルボキシル化することにより生成されます。この過程はアセチル CoA カルボキシラーゼが触媒しますが、ビオチンを補酵素として必要とします。
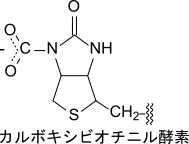
まず、ATP を消費して炭酸水素イオンがリン酸化され、カルボキシリン酸中間体が生成されます。次いで、ビオチンに炭酸が付加されることによりカルボキシビオチニル酵素となります(なお、ビオチンは酵素のリシン残基を介して酵素と結合しています)。アセチル CoA の α 炭素からプロトンが抜きとられることでアセチル CoA はエノラートイオンとなり、炭酸を求核攻撃することにより結合してマロニル CoA が生成されます(図5)。なお、エノラート形成からマロニル CoA 生成までの過程は協奏反応(concerted reaction)として知られています。協奏反応とは結合形成と結合切断が同時に起こる(時間的に重なり合う)反応形式を指します。したがってエノラートイオンは瞬間的にしか存在できないと考えられています。
生成されたマロニル CoA はマロニル/アセチル CoA-ACP アシルトランスフェラーゼドメインの作用により ACP に転移されてマロニル ACP となり、脂肪酸シンターゼに固定されます。
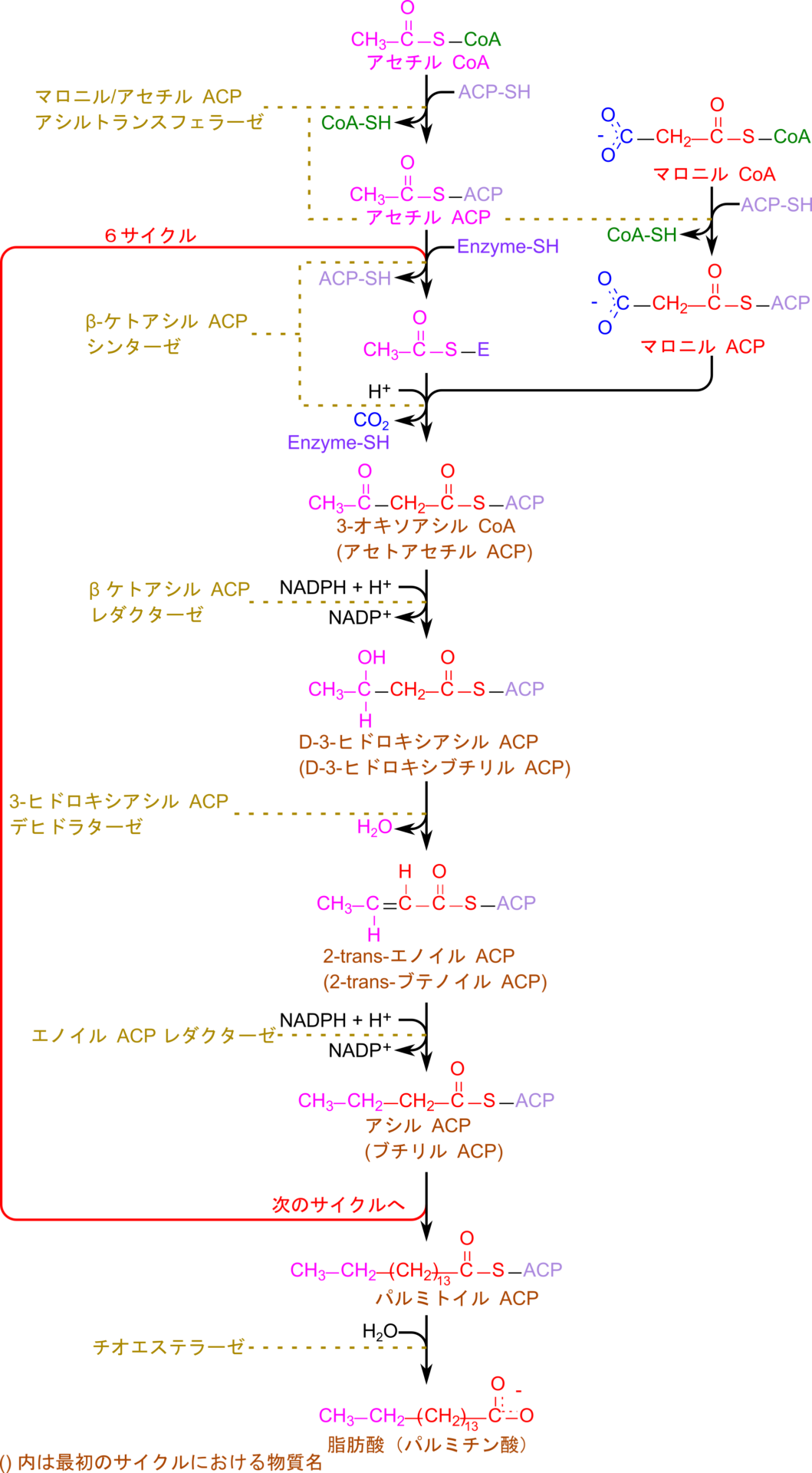
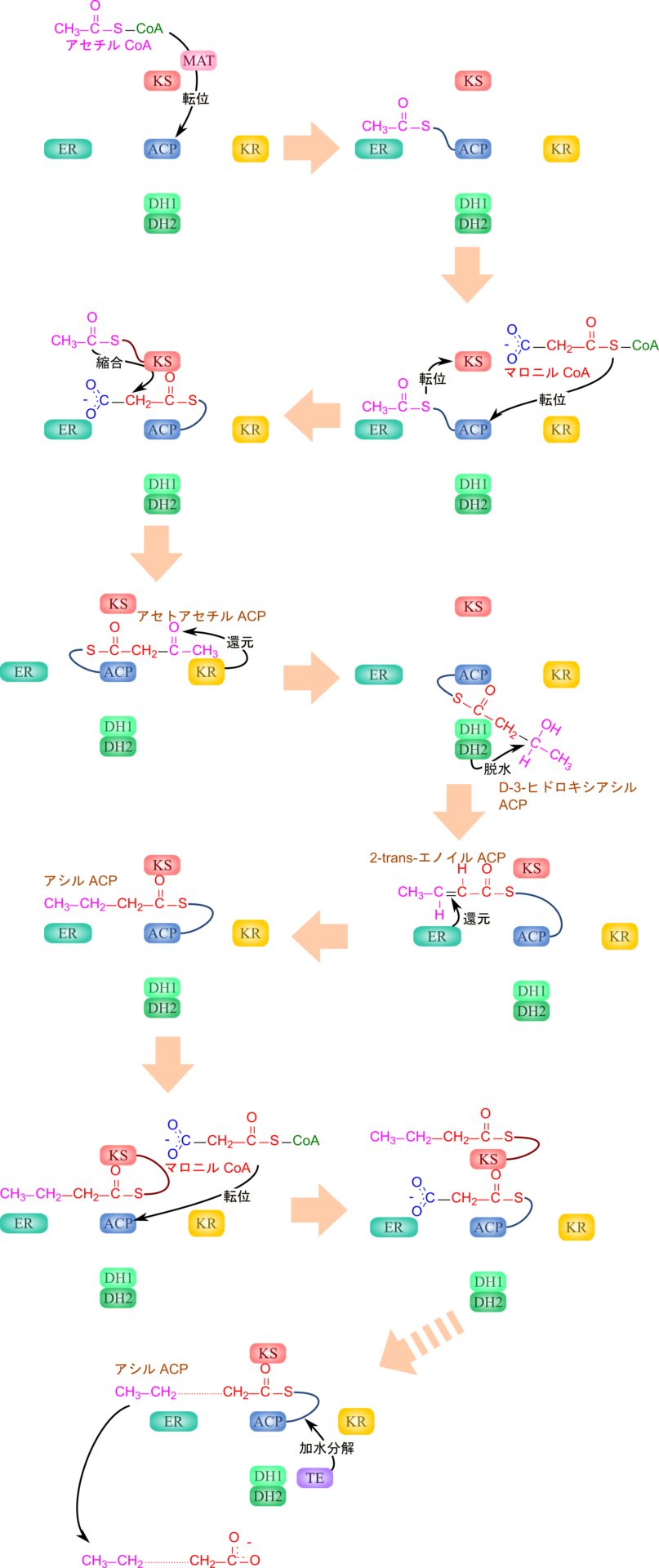
脂肪酸伸長反応
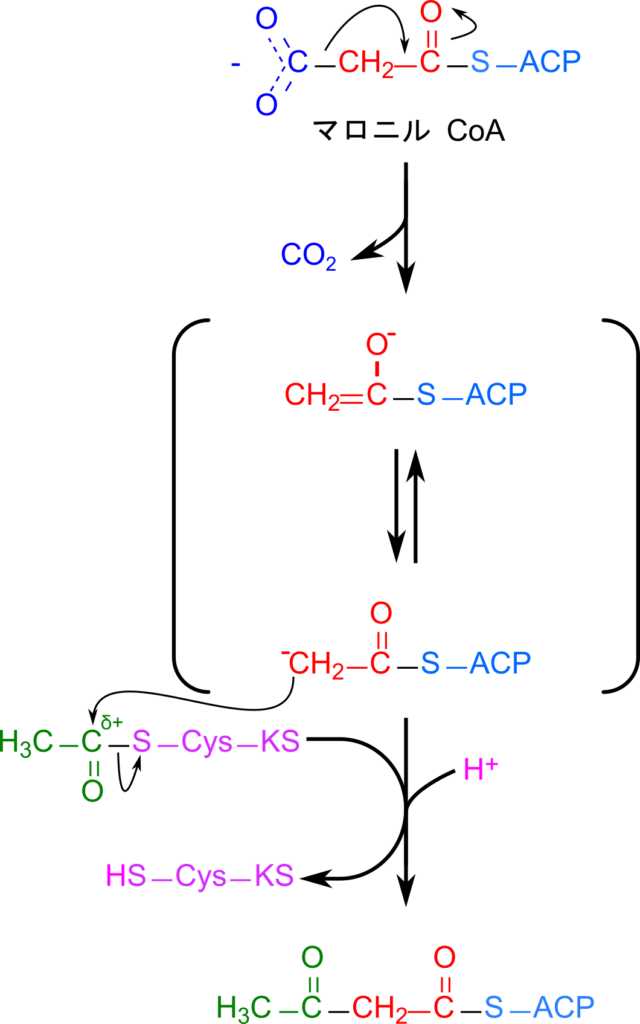
アセチル基はアセチル CoA から ACP にマロニル/アセチル CoA-ACP アシルトランスフェラーゼドメインの作用により転移させられます。その後、 β ケトアシル ACP シンターゼドメインの作用によりアセチル基は ACP から β ケトアシル ACP シンターゼドメインのシステイン残基のチオール基に転移させられます。さらに、マロニル CoA が脱炭酸されることにより生じるカルボアニオンがアセチル基のカルボニル基を求核的に攻撃して結合し縮合します。この反応も β ケトアシル ACP シンターゼドメインにより触媒されます(図6)。
この後、アセトアセチル ACP の 3 位のカルボニル基が β ケトアシル ACP レダクターゼドメインの作用を受けて還元されて、水酸基に変換されます。この際に NADPH + H+ が消費されて NADP+ に変換されます。次いで、3-ヒドロキシアシル ACP デヒドラターゼドメインの作用により Δ2-3 位から水が脱離して 2‐trans-エノイル ACP となり、最後に、エノイル ACP レダクターゼが NADPH を消費して二重結合を還元し、炭素数が2伸長されたアシル ACP が生成されます。
アシル ACP は再びβ ケトアシル ACP シンターゼドメインのチオール基に転移させられ、後はマロニル ACP の縮合反応から繰り返されていくことになります。その後、アセチル ACP 部分(図7のピンク色の部分)はサイクルを一つこなす毎に炭素数が2ずつ増えていきます。最終的に炭素数が16に達するとチオエステラーゼドメインの作用によりアシル ACP が加水分解を受けて脂肪酸部分が遊離します。このときにチオエステラーゼドメインは脂肪酸の長さを計る定規のような役割も担っています。

脂肪酸シンターゼの構造
これまでも記述している通り、脂肪酸シンターゼは構造的、機能的に独立した部分構造であるドメイン構造を複数内包する多彩な活性を持つタンパク質です。ここでは脂肪酸シンターゼの構造についてみていきましょう。
脂肪酸シンターゼの一次構造についてみていきます。ドメイン構造は図8に示すように、N末端側から以下の順に並んでいます。
- β-ケトアシル-ACP シンターゼ(β-ketoacyl-ACP synthase; KS)
- マロニル/アセチル ACP アシルトランスフェラーゼ(malonyl/acetyl ACP acyltransferase; MAT)
- 3-ヒドロキシアシル ACP デヒドラターゼ1(3-hydroxyacyl ACP dehydratase1; DH1)
- 3-ヒドロキシアシル ACP デヒドラターゼ2(3-hydroxyacyl ACP dehydratase2; DH2)
- 偽メチルトランスフェラーゼ(pseudo-methyltransferase; ψ-MT)※
- 偽ケト ACP レダクターゼ(pseudo-ketoreductase; ψ-KR)※
- エノイル ACP レダクターゼ(enoyl ACP reductase; ER)
- β-ケトアシル ACP レダクターゼ(β-ketoacyl ACP reductase; KR)
- アシルキャリアタンパク質(acyl carrier protein; ACP)
- チオエステラーゼ(thioesterase; TE)
※偽メチルトランスフェラーゼと偽ケト ACP レダクターゼは機能を失った構造で厳密にはドメイン構造とは言えませんが、配列が類似しているため偽ドメインとして記載しています。
立体構造を考慮して模式的に配置した図が図8のBです。脂肪酸シンターゼは単体では機能を発揮することはできず、ホモダイマー(脂肪酸シンターゼ2分子が相互作用している状態)となって機能します。
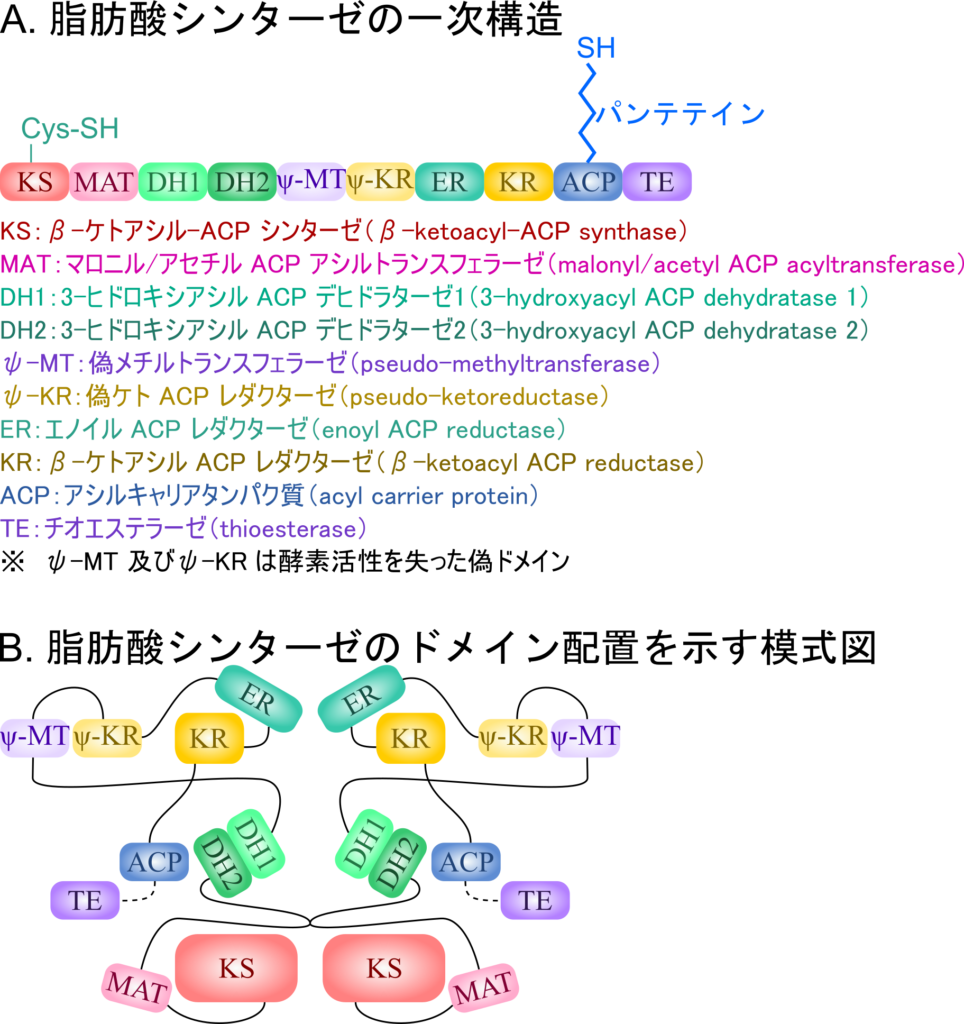
アセチル CoA やマロニル CoA は ACP に転移させられ、アセチル ACP やマロニル ACP となります。その後、脂肪酸の伸長反応は脂肪酸シンターゼを構成する各ドメインが触媒するわけですが、ACP がアセチル基やマロニル基と結合しているホスホパンテテインは柔軟で様々な方向に向くことが可能です。この特性は ACP と結合している基質が各反応を触媒するドメインの近傍に配置することを可能にしています(図9)。このように、ACP は基質を固定するだけでなく、基質が適切な位置に配置できるように制御する役割も担っています。
脂肪酸合成の化学量論
炭素数が偶数の脂肪酸合成のサイクル数は以下数式で算出することができます。最初にアセチル CoA が炭素2個を供給しますから、炭素数全体からこの2個分を除外する必要があります。1サイクル当たり2個ずつ伸長するわけですので2で割ればサイクル数が算出できます。![]()
なお、ほとんどの場合は合成される脂肪酸は偶数ですが、極めて稀なケースで炭素数が奇数の脂肪酸が合成される場合もあります。この場合は最初に供給される分子がアセチル CoA ではなくプロピオニル CoA(炭素数3)となります。したがって上述の式は以下のように変更されます。![]()
冒頭でも記載した通り、脂肪酸合成ではパルミチン酸が生成されます。そこでパルミチン酸を例にサイクル数と必要となる分子について考察します。パルミチン酸は炭素数が 16 ですので上の式に当てはめると、7 サイクルが必要となります。
各段階における反応を見ていきましょう。
アセチル CoA カルボキシラーゼが触媒する反応
アセチル CoA + CO2 + ATP → マロニル CoA + ADP + Pi + H+
脂肪酸シンターゼが触媒する反応
マロニル/アセチル ACP アシルトランスフェラーゼドメインが触媒する反応
アセチル CoA + ACP → アセチル ACP + CoA
———-(ここから繰り返し)———-
マロニル CoA + ACP → マロニル ACP + CoA
β-ケトアシル ACP シンターゼドメインが触媒する反応
マロニル ACP + アセチル ACP※ → アセトアセチル ACP + CO2 + ACP
※ここでは1サイクル目として記載していますのでアセチル ACP としています。
それ以降はは1サイクル前に合成されたアシル ACP である点に注意です。
2 サイクル目ならブチリル ACP(炭素数 4)など。
β-ケトアシル ACP レダクターゼドメインが触媒する反応
アセトアセチル ACP + NADPH + H+ → D-3-ヒドロキシアシル ACP + NADP+
3-ヒドロキシアシル ACP デヒドラターゼドメインが触媒する反応
D-3-ヒドロキシアシル ACP → 2-trans エノイル ACP + H2O
エノイル ACP レダクターゼドメインが触媒する反応
2-trans エノイル ACP+ NADPH + H+ → アシル ACP + NADP+
———-(ここまで繰り返し)———-
パルミトイルチオエステラーゼが触媒する反応
パルミトイル ACP + H2O → パルミチン酸 + ACP
パルミチン酸の生成をまとめると以下の式で表せます(繰り返す部分は7倍する必要がある点に注意です)。
アセチル CoA + 7マロニル CoA + 14NADPH + 14H+ →
パルミチン酸 + 7CO2 + 14NADP+ + 8CoA + 6H2O
さらに、7 分子のマロニル CoA は 7 分子のアセチル CoA から合成されます。
7アセチル CoA + 7CO2 + 7ATP → 7マロニル CoA + 7ADP + 7Pi + 7H+
このことを合わせて考慮するとパルミチン酸の生成は以下の式で表すことができます。
8アセチル CoA + 14NADPH + 7ATP + 7H+ →
パルミチン酸 + 14NADP+ + 8CoA + 6H2O + 7ADP + 7Pi
※反応をまとめる際に、アシル ACP はサイクルが進行するにしたがって次々に変化していく点に注意です。途中で生成される各アシル ACP は次のサイクルで消費されるので、反応全体をまとめてしまうと結局アセチル ACP が利用され、パルミチン酸が生成される部分だけが残ります。
また、プロトンの数はどの反応でプロトンをカウントするかによって文献ごとでも異なります。
練習問題
以下の図の [1] ~ [3] に当てはまる構造を選べ
![脂肪酸合成の反応図。図中に [1], [2], [3] の枠が示されている。](https://www.lifescience-note.net/wp-content/uploads/2025/10/fattyacid_synthesis_question-e1759845008646.png)
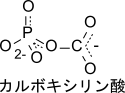
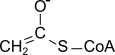
問題
パルミチン酸 1 分子を生成する場合に必要となる ATP の分子数を答えよ
「脂肪酸合成はβ酸化の逆再生ではない」――本稿ではこの起点から、反応の場・キャリア(ACP/CoA)・伸長単位(マロニル-ACP)・補酵素(NADPH)という相違点の骨格を押さえ、マロニルCoA形成、脂肪酸シンターゼによる2炭素ずつの伸長サイクル、そしてパルミチン酸生成の化学量論までを一気通貫で整理しました。
図表とともに要点へ戻れば、「なぜ2炭素ずつ伸びるのか」「なぜNADPHなのか」「なぜACPなのか」など、脂肪酸合成のポイントが深く理解できるはずです。今後の学習にもぜひ役立ててください。
参考文献
- 島原健三 (1991). 概説 生物化学. 三共出版. pp. 190-207
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp. 597-632
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp.440-476
- Smith, S., & Tsai, S.-C. (2007). The type I fatty acid and polyketide synthases: a tale of two megasynthases. Natural Product Reports, 24(5), 1041–1072. https://doi.org/10.1039/b603600g
- Maier, T., Leibundgut, M., & Ban, N. (2008). The Crystal Structure of a Mammalian Fatty Acid Synthase. Science, 321(5894), 1315–1322. https://doi.org/10.1126/science.1161269
- UCHIYAMA, M. (1974). Biosynthesis and Organic Synthesis of Fatty Acids. Journal of Japan Oil Chemists’ Society, 23(10), 599–604. https://doi.org/10.5650/jos1956.23.599