芳香族アミノ酸生合成の出発物質はホスホエノールピルビン酸とエリトロース-4-リン酸という炭素数が3~4に過ぎない化合物です。この単純な化合物が複雑な芳香族アミノ酸になっていく過程には生命の巧妙さが見て取れます。今回は芳香族アミノ酸の生合成経路だけでなく基質チャネリングのような生化学で重要な概念もわかりやすく解説します。
Contents
芳香族アミノ酸の生合成の概要
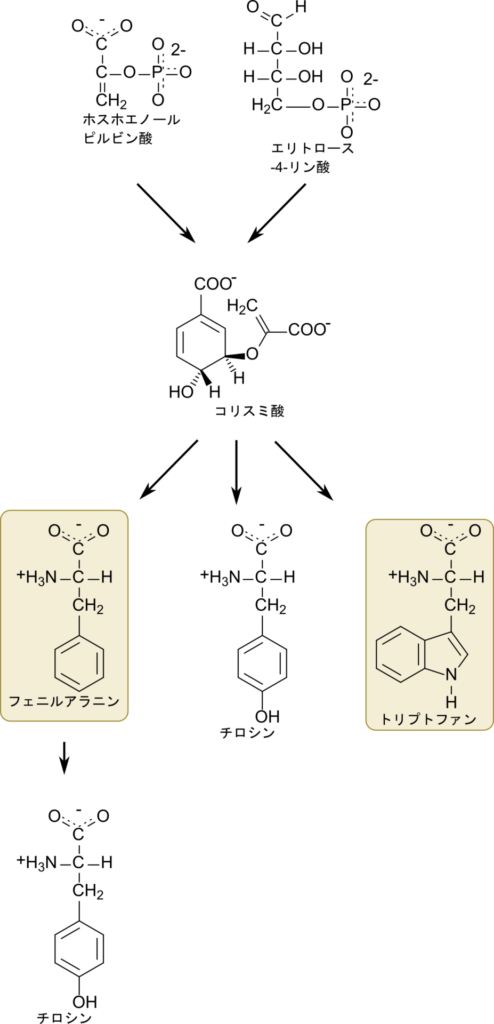
芳香族アミノ酸の生合成は前半と後半に分けて理解しましょう。芳香族アミノ酸ではまずコリスミ酸という六員環を持つ化合物を生成します。このコリスミ酸が芳香族アミノ酸―フェニルアラニン、チロシン、トリプトファン―の生合成の起点となります(図1)。したがって、芳香族アミノ酸の生合成ではまずホスホエノールピルビン酸2分子とエリトロース-4-リン酸からコリスミ酸が合成される段階とコリスミ酸から各芳香族アミノ酸が合成される段階に分けて理解するとわかりやすいと思います。
コリスミ酸の生合成の後は、チロシンとフェニルアラニンの生合成経路であるプレフェン酸経路(prephenate branch)とトリプトファンの生合成経路に分かれます。チロシンとフェニルアラニンの生合成はプレフェン酸の合成に始まり、その後互いによく似た経路をたどります。一方でトリプトファンの生合成はさらに複雑な経路を経由します。
今回はコリスミ酸の合成経路、フェニルアラニンとチロシンの生合成経路、トリプトファンの生合成経路に分けて紹介します。
芳香族アミノ酸生合成の第一段階―コリスミ酸の生合成
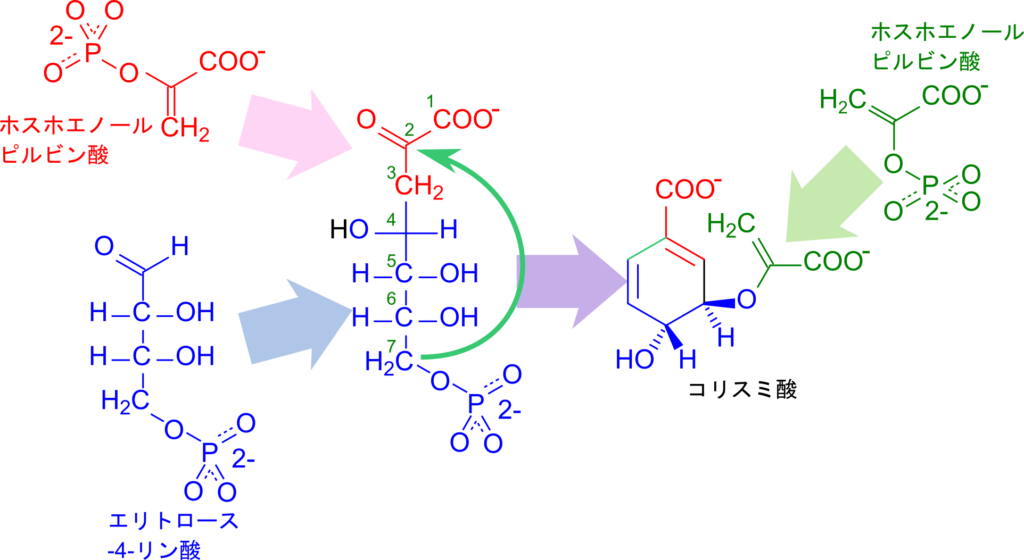
コリスミ酸の生合成を見ていく前に出発物質であるホスホエノールピルビン酸、エリトロース-4-リン酸の構造とこれらの分子が会合してできる 3-デオキシ-アラビノ-ヘプツロソン酸-7-リン酸の構造、さらにコリスミ酸の構造を比較してみましょう(図2)。コリスミ酸は六員環を持つ炭素数が10の化合物です。そこで、ホスホエノールピルビン酸とエリトロース-4-リン酸が会合することで炭素数7の 3-デオキシ-アラビノ-ヘプツロソン酸-7-リン酸が生成します。これでもまだ炭素数が3足りませんが、これは後程供給されますので、いったん置いておきます。まずは六員環を与える反応についてみていきましょう。 3-デオキシ-アラビノ-ヘプツロソン酸-7-リン酸の7位の炭素が2位の炭素と結合を形成すると、六員環が生成されます。これで六員環がえられましたが、側鎖のピルビン酸部分がまだ足りません。そこで、ホスホエノールピルビン酸と会合することで側鎖のピルビン酸部分が付加されて、コリスミ酸が生成されます。では各反応を詳しく見ていきましょう。
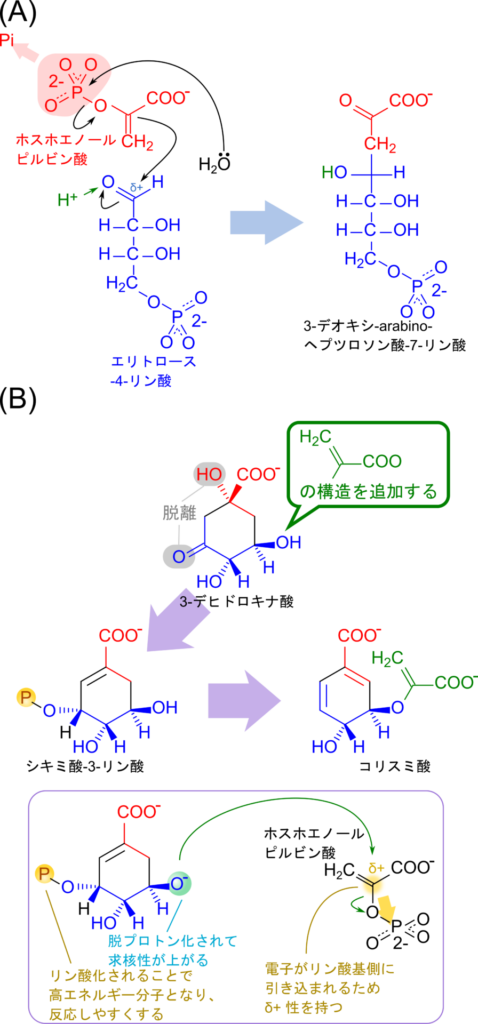
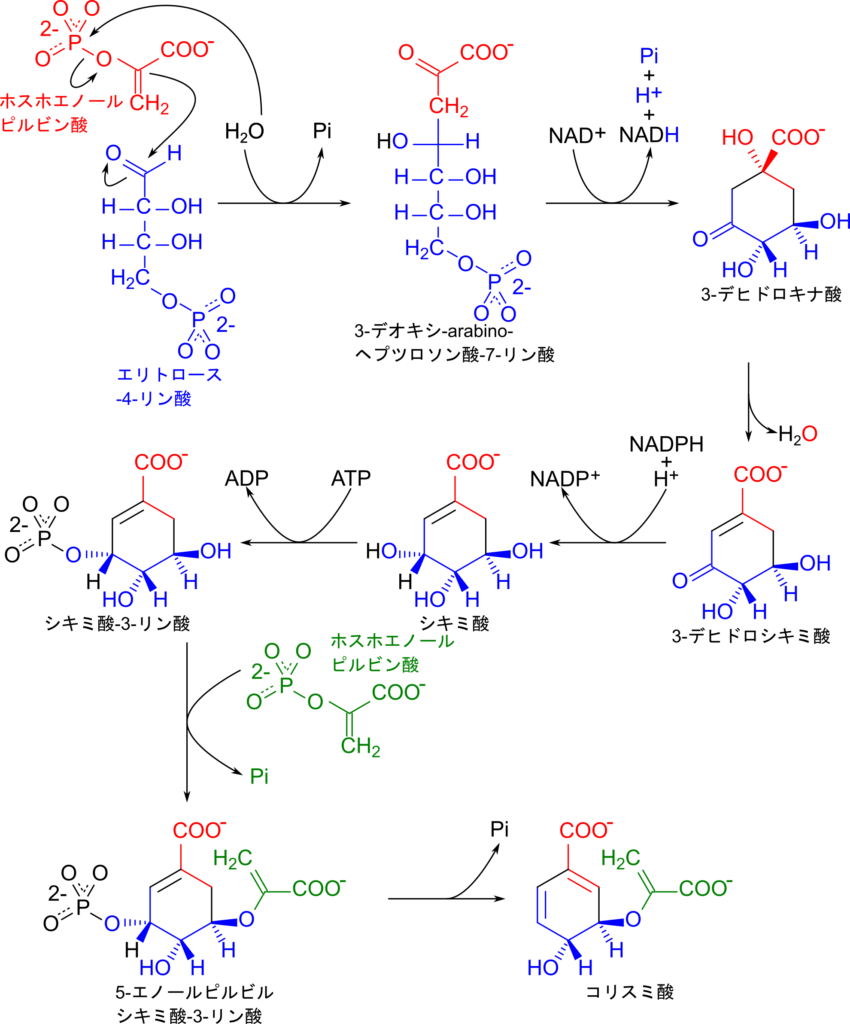
コリスミ酸の生合成ではホスホエノールピルビン酸とエリトロース-4-リン酸が会合して 3-デオキシ-アラビノ-ヘプツロソン酸-7-リン酸を生成する反応が第一ステップです。この反応はホスホエノールピルビン酸が加水分解を経て脱リン酸化されることからはじまります。こうして得られるエノール型のピルビン酸はエリトロース-4-リン酸の1位の炭素(ホルミル基;CHO基の炭素原子)を求核的に攻撃することで結合を形成します。するとホルミル基の π 電子は酸素側に移行し、プロトン化されて水酸基となります。こうして、 3-デオキシ-アラビノ-ヘプツロソン酸-7-リン酸が生成されます(図3.A)。
その後7位の炭素が2位の炭素(カルボニル基;C=O)と結合を形成すると六員環が生成されます。この時にリン酸が脱離して 3-デヒドロキナ酸が生成されます。
ここで、3-デヒドロキナ酸とコリスミ酸の構造を比較してみます(図3.B)。3-デヒドロキナ酸にピルビン酸を導入し、水酸基とオキソ基を除去するとコリスミ酸となります。ところで、シキミ酸-3-リン酸は5位の水酸基からプロトンが脱離し水酸基を -O– に変換します。ホスホエノールピルビン酸は求電子性を持つため、脱プロトン化された水酸基がターゲットとなり、ピルビン酸が付加されます。以上のことを踏まえて詳細を見ていきましょう。
この生合成経路は、まず 3-デヒドロキナ酸は水として1位の水酸基が脱離して、3-デヒドロシキミ酸を生成します。さらに、ホスホエノールピルビン酸と会合することでピルビン酸を導入します。この反応では、シキミ酸-3-リン酸の 5 位の水酸基からプロトンが除去されてオキシアニオン (-O–) を生成します。このオキシアニオンはホスホエノールピルビン酸の δ+ 性を有する炭素を求核的に攻撃します。この結果、ホスホエノールピルビン酸とシキミ酸が結合し、ホスホエノールピルビン酸からリン酸が脱離します。この時、シキミ酸にリン酸基が結合していることにより、シキミ酸-3-リン酸は高エネルギー分子となり、この反応が進みやすくなっています。こうして、5-エノールピルビルシキミ酸-3-リン酸が生成されます。最後に3位のリン酸基が脱離するとコリスミ酸が生成されます(図4)。
ここまでで、芳香族アミノ酸の生合成の前半が終わりました。さらに後半についてみていきましょう。
芳香族アミノ酸の生合成―各芳香族アミノ酸の生合成
チロシンとフェニルアラニンの生合成経路(プレフェン酸経路)
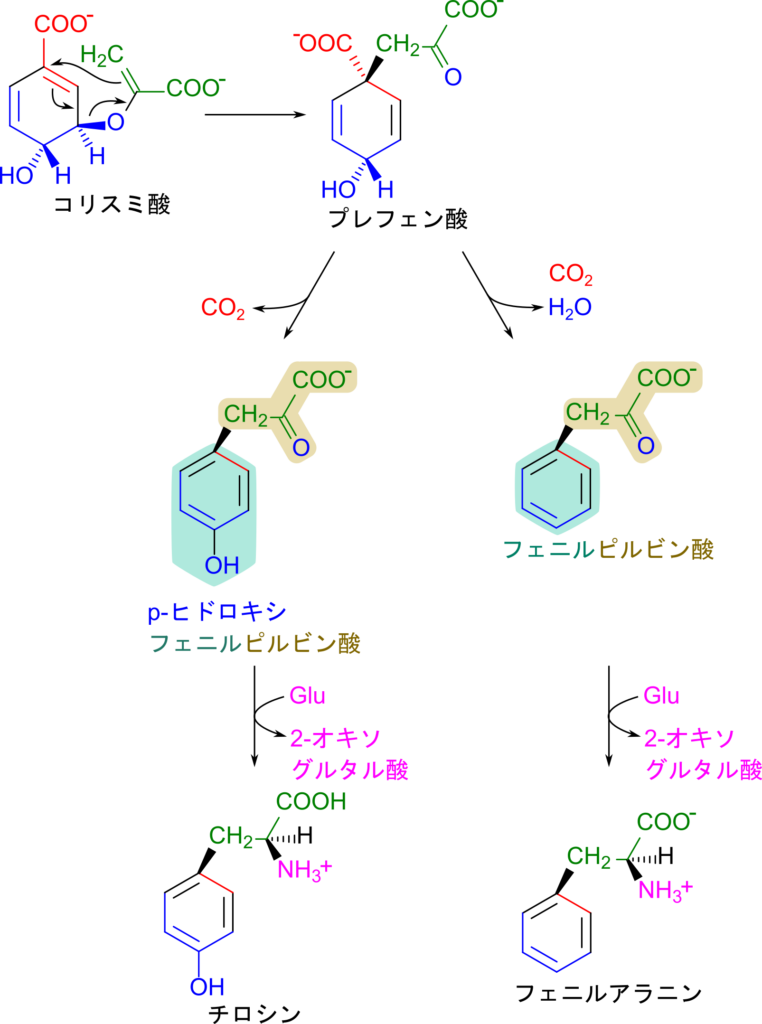
チロシンとフェニルアラニンの生合成経路はプレフェン酸を生成中間体として合成するためプレフェン酸経路と呼ばれます。この反応はムターゼの作用により触媒され、エノール型のピルビン酸部分が転位されてプレフェン酸が生成されます。この時にピルビン酸部分はエノール型からケト型に転換されます。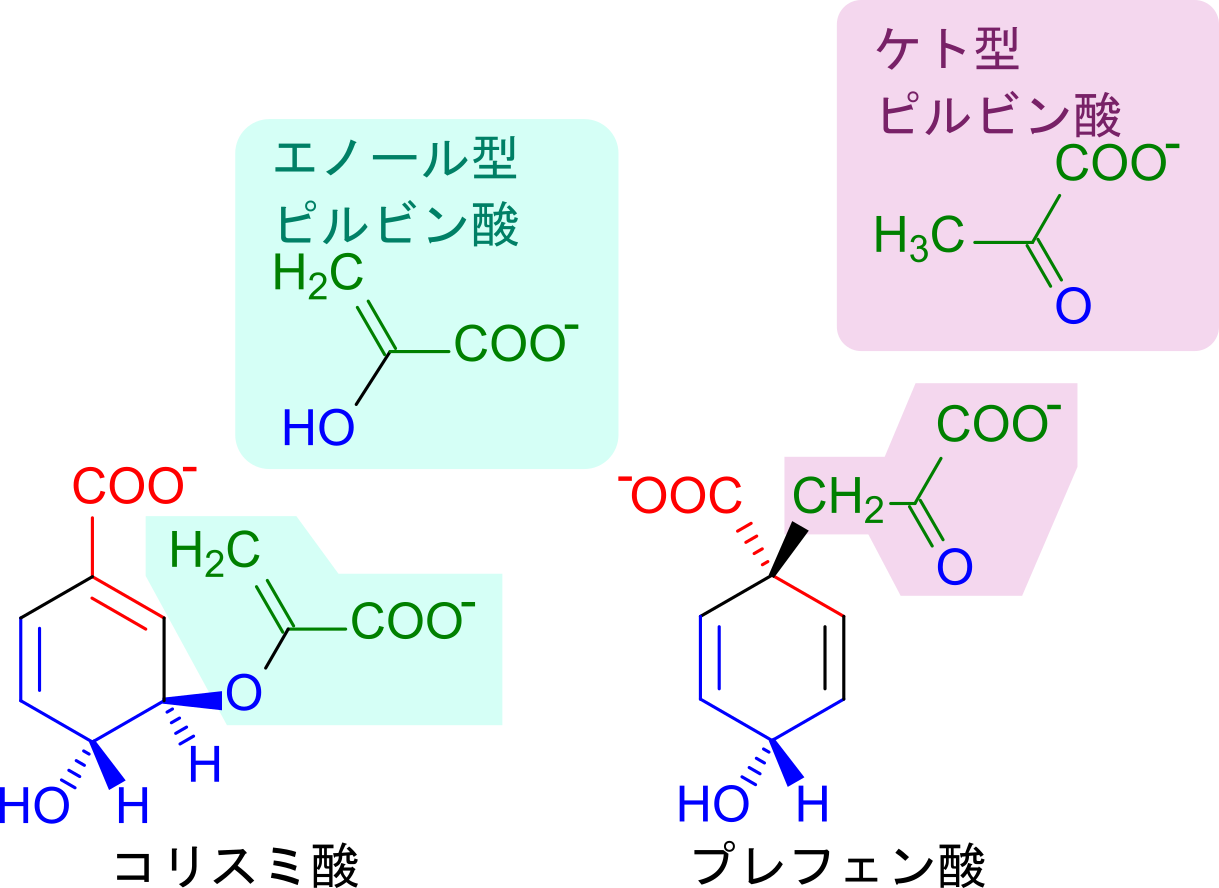
プレフェン酸はチロシンやフェニルアラニンとかなり近い構造をしています。
カルボキシル基を炭酸として脱離させると p-ヒドロキシフェニルピルビン酸が生成されます。p-ヒドロキシフェニルピルビン酸はチロシンを脱アミノした構造をしており、あとはグルタミン酸によるアミノ基転位を受けるとチロシンが生成されます。
一方でフェニルアラニンにするにはパラ位の水酸基が邪魔ですね。ですので、この水酸基とカルボキシル基を脱離させます。するとフェニルアラニンを脱アミノした α-オキソ酸であるフェニルピルビン酸が生成されます。あとはグルタミン酸によるアミノ基転位を受けるとフェニルアラニンが生成されます。
トリプトファンの生合成経路
トリプトファンの生合成経路の詳細
コリスミ酸からトリプトファンの生合成について考えるにあたり、このままでは少し複雑なので、トリプトファンの各置換基がどの分子から供給されるのかについてみていきましょう(図6)。
- トリプトファンの六員環部分 :コリスミ酸の六員環由来
- トリプトファンの側鎖アミノ基 :グルタミンから転位
- トリプトファンの五員環の炭素二つ:ホスホリボシル二リン酸(PRPP)由来
- トリプトファンの主鎖部分 :セリン由来
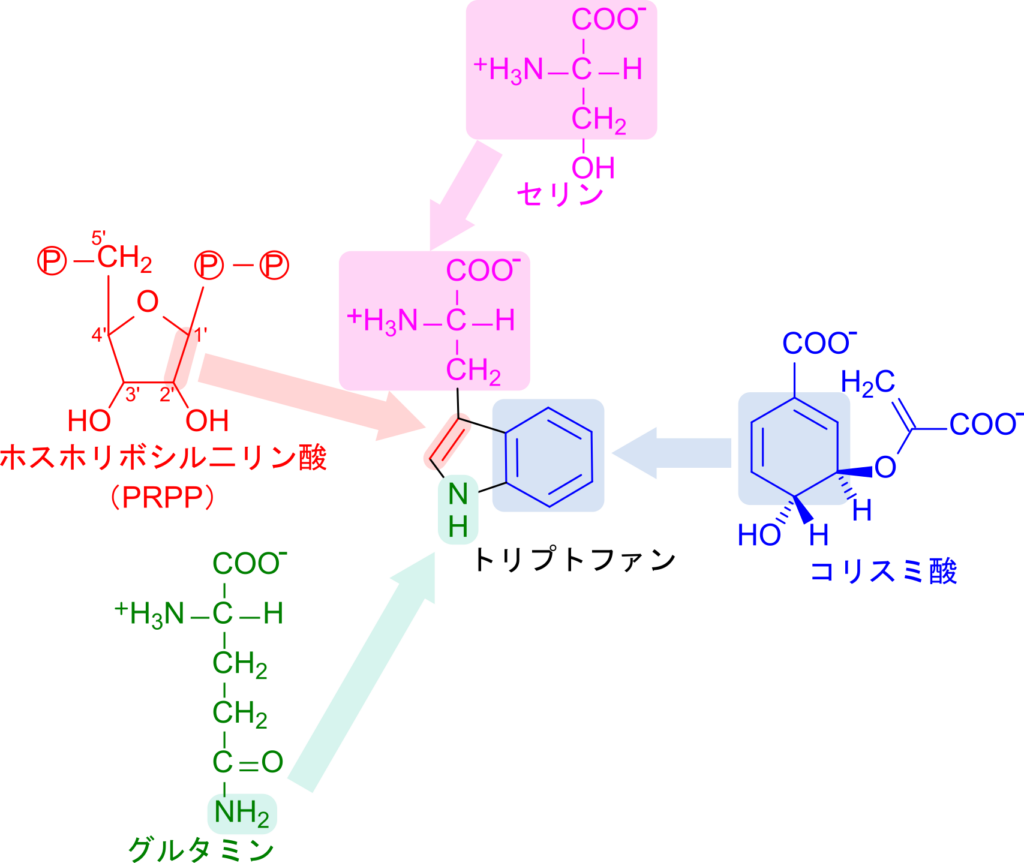
トリプトファンの生合成経路はコリスミ酸の六員環にこれらの置換基が付加されていく過程とみると理解しやすいと思います。それでは具体的に各ステップを見ていきましょう。
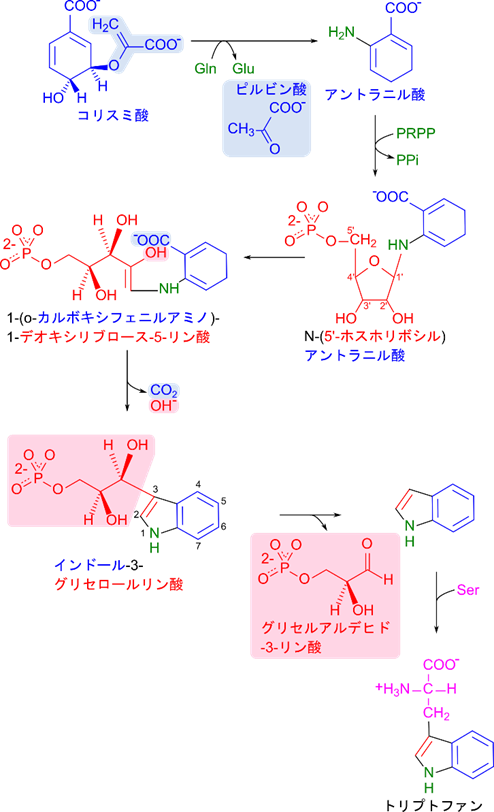
トリプトファンの生合成経路ではまず、コリスミ酸にグルタミンからアミノ基が供給され、次いでピルビン酸部分が遊離します。この結果、アントラニル酸が生成されます。次いで、ホスホリボシル二リン酸がアミノ基に付加されたのち、リボースが開環します(1-(o-カルボキシフェニルアミノ)-1-デオキシリブロース-5-リン酸)。リボースの 2′ 位炭素が六員環の1位の炭素(カルボキシル基が結合している炭素)と結合を形成して、五員環を形成します。この時、アントラニル酸のカルボキシル基が炭酸として脱離するとともにホスホリボシル二リン酸の 2′ 位の水酸基も脱離します。こうしてインドール環が形成されます。ただし、PRPP に由来するグリセロールリン酸部分が余分なので次のステップで除去されてインドール環が遊離します。インドール環はトリプトファンの側鎖部分に相当します。ここに主鎖部分を付加するとトリプトファンとなります。そこで、セリンを付加して主鎖部分を供給し、トリプトファンが生成されます。
ここまでが、トリプトファンの生成経路です。トリプトファンの生合成経路にはこれまでに解説したほかに注目するべき点がいくつかあります。次の項目からはこれらのポイントについてみていきましょう。
インドール環とセリンの会合はピリドキサールリン酸(pyridoxal phosphate; PLP)を介して行われる
インドール環にセリンが付加する反応はトリプトファンシンターゼによって触媒される反応です。この酵素は内部にピリドキサールリン酸(pyrdoxal phosphate; PLP)を持っており、インドール環にセリンが付加する反応に関与しています。PLP は以前にグルタミン酸からのアミノ基転位反応に関与する補酵素として紹介しました(詳細はこちら)。PLP はビタミン B6 として知られており、アミノ基転位反応以外にも、脱炭酸や、グリコーゲンを分解してグルコース-1-リン酸を生成する反応など様々な反応に関与します。ここではインドール環にセリンを付加する反応について紹介します。
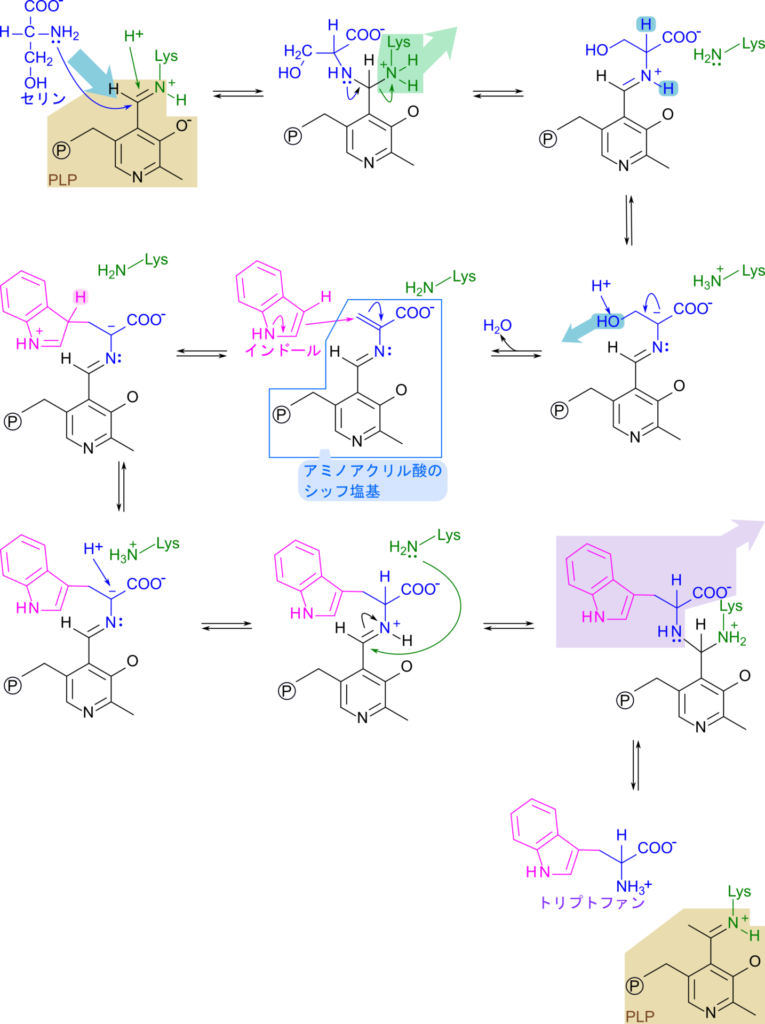
まずは概要について説明します。PLP は一度セリンと結合し、アミノアクリル酸(CH2=CHCOOHと窒素原子をもつ分子)を生成します。このアミノアクリル酸はシッフ塩基(C=N を有する化合物、容易に還元される性質がある)でもあり、反応性が高い物質です。したがって、容易にインドール環と反応して結合を形成し、トリプトファンを生成します(図8)。では詳細に見ていきましょう。
PLP は酵素のリシン残基と結合した状態で存在します。ここにセリンが付加すると、リシンがいったん遊離します(図8の1~3段階目)。その後、セリンから脱水により水酸基が脱離してアミノアクリル酸が生成されます(図8の4~5段階目)。このアミノアクリル酸の生成がセリンとインドール環の会合のカギとなります。アミノアクリル酸はシッフ塩基でもあり、還元されやすいため反応性が高く、容易にインドール環と結合します(図8の5~6段階目)。その後、水素化されるとトリプトファンの構造が出来上がります(図8の7~8段階目)。一方で、酵素中のリシンが PLP に結合し、リシンと交換するような形でトリプトファンが遊離して反応が終了します(図8の8~10段階目)。このように、PLP はトリプトファンの生合成においても重要な役割を担っており、PLP の多彩な機能の一端を垣間見ることができます。
セリンの付加反応は基質チャネリングを介して行われる
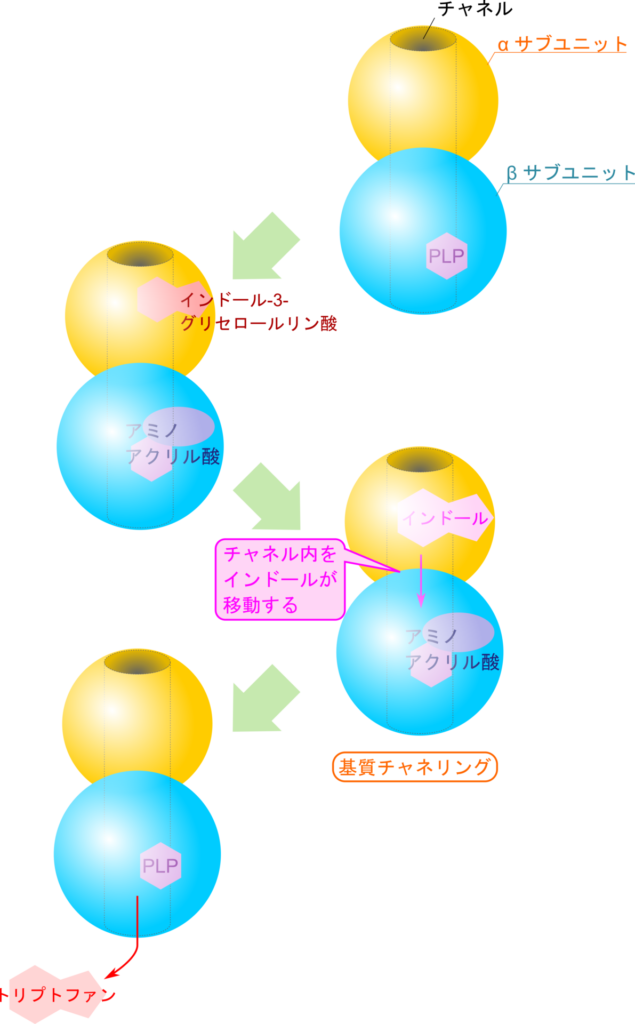
トリプトファンシンターゼは α サブユニット2分子と β サブユニット2分子から構成されます(α2β2 と表記します)。α サブユニットではインドール-3-グリセロールリン酸からインドールが遊離する反応が行われます。一方で、β サブユニットでは PLP が存在し、セリンの付加反応が行われます(この過程は前項目を参照してください)。
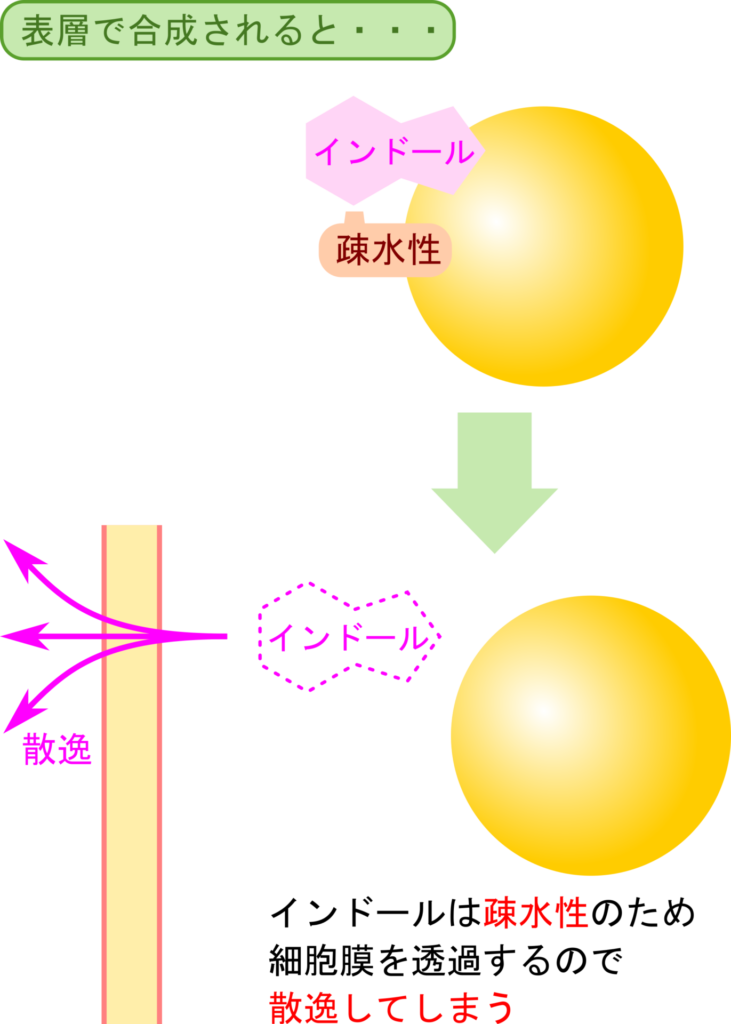
ところで、α サブユニットで生成されるインドールは疎水性のため、そのままでは細胞膜を透過して散逸してしまいます。生成するそばから散逸してしまうのではセリンを付加してトリプトファンを産生することはできません。このため、インドールの生成からトリプトファンの生成までの段階には工夫が必要です(図9)。
トリプトファンシンターゼには α サブユニットと β サブユニットを貫通するようにトンネル状の構造(チャネル)が存在しています。インドールの生成からトリプトファンの生成までの反応はこのチャネル内で行われます。PLP がセリンと結合し、アミノアクリル酸が生成すると、インドールがインドール-3-グリセロールリン酸から遊離します。生成されたインドールはチャネル内を通過して β サブユニットに渡されて、アミノアクリル酸と反応してトリプトファンの生成が行われます。この過程ではインドールは酵素外に一切出ることなく、二つの反応を経てトリプトファンの生成が可能となります。このように基質が酵素内のチャネルを通過して複数の反応を経る過程のことを基質チャネリング(substrate channeling)といいます。基質チャネリングには以下のような利点があります(図10)。
- 基質が外部と接触することによる好ましくない事態を避けられます
e.g. 今回の例では、基質の散逸を防止できます - 二つの活性中心を速やかに基質が移動することが可能となるため反応速度がかなり上昇します
基質チャネリングに加えて、これらの反応が厳密に制御されることで、さらに効率を高めると同時にインドールの散逸のリスクを抑えています(図11)。
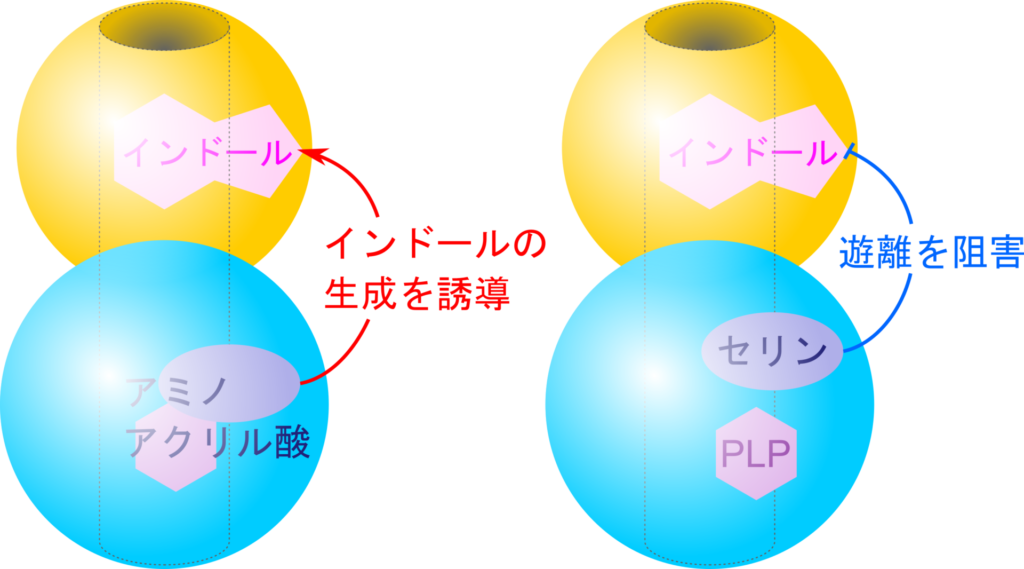
インドール生成はセリンが存在している間は行われないようになっています。セリンが存在するということは PLP とセリンの会合は行われておらず、アミノアクリル酸はまだ生成していないことになります。この状態でインドールが生成してもセリン付加の準備が整っていないので反応を進めることはできません。このため、セリンが存在するとインドール生成は抑制されます。
一方で、アミノアクリル酸が生成されるとトリプトファン合成の準備ができたことになるのでインドールの生成が誘導されます。
このように、インドール生成はアミノアクリル酸生成と連動するように制御されることにより、インドール生成からトリプトファン生成までの流れはスムーズに進むようにコントロールされているわけです。
今回は芳香族アミノ酸の生合成について解説しました。芳香族アミノ酸は、アミノ酸の中でも特に複雑な構造を持ちますが、その生合成経路の出発物質はホスホエノールピルビン酸とエリトロース-4-リン酸というとても単純な化合物です。単純な化合物から複雑な化合物が生成される過程には、生命の巧妙さが表れています。また、芳香族アミノ酸の生合成経路には、PLPの作用や基質チャネリングといった、他の代謝経路でも重要なメカニズムが含まれています。このように、芳香族アミノ酸の生合成経路を理解することは、生化学のより深い理解につながります。ぜひこの記事を使って理解を深めてください。
参考文献
- 島原健三 (1991). 概説 生物化学. 三共出版. pp. 208-223
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp.665-693
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp.496-503
- KEGG PATHWAY DATABASE. 2025-03-03. https://www.genome.jp/kegg/pathway.html
- Caulkins, B. G., Yang, C., Hilario, E., Fan, L., Dunn, M. F., & Mueller, L. J. (2015). Catalytic roles of βLys87 in tryptophan synthase: 15N solid state NMR studies. Biochimica et Biophysica Acta (BBA) – Proteins and Proteomics, 1854(9), 1194–1199. https://doi.org/10.1016/J.BBAPAP.2015.02.003
- Dong, Y., Ng, E., Lu, J., Fenwick, T., Tao, Y., Bertain, S., … Siehl, D. (2019). Desensitizing plant EPSP synthase to glyphosate: Optimized global sequence context accommodates a glycine-to-alanine change in the active site. Journal of Biological Chemistry, 294(2), 716–725. https://doi.org/10.1074/jbc.RA118.006134