2-オキソグルタル酸から生合成されるアミノ酸には、アミノ基の供給源ともなるグルタミン酸やグルタミン、プロリンのような環状構造をもつアミノ酸やアルギニンのような多数の窒素を含むものなど少し特殊なアミノ酸も含まれています。本記事では、これらのグルタミン酸・グルタミン・プロリン・アルギニンの生合成をわかりやすく解説します。
Contents
2-オキソグルタル酸に由来するアミノ酸の生合成の概要
2-オキソグルタル酸がアミノ基転位を受けるとグルタミン酸が生成されます。この反応はアンモニウム塩の取り込みとしても重要な反応です(詳細はこちらで解説しています)。グルタミン酸はさらに ATP を消費してアンモニウム塩を受け取りグルタミンに変換されます。一方で、グルタミン酸はプロリンやアルギニンの前駆体ともなっています。プロリンとアルギニンは共通の代謝中間体であるグルタミン酸-γ-セミアルデヒド(グルタミン酸の側鎖カルボニル基がホルミル基に変換された構造)を生成したのち、プロリンの生合成と尿素回路を介したアルギニンの生合成経路に分岐します。このことから、この記事ではグルタミン酸の生合成、グルタミンの生合成、プロリン・アルギニンの生合成に分けて解説します。

グルタミン酸とグルタミンの生合成
グルタミン酸の生合成は2-オキソグルタル酸がアミノ基転位を受けることで行われます。この反応はアンモニウム塩をアミノ基として取り込む反応としても重要です。
2-オキソグルタル酸のカルボニル基は δ+ 性を持っているため、(非共有電子対を持つ)アンモニウム塩の窒素から求核的に攻撃されます。その結果、イミン(N=C)を形成しますが、イミンはシッフ塩基とも呼ばれ容易に還元・水素化されてアミンに変換されます。この還元反応には酸化還元反応に関与する補酵素である NADH あるいは NADPH が関与して行われます。この結果、グルタミン酸が生成されます(図2)。
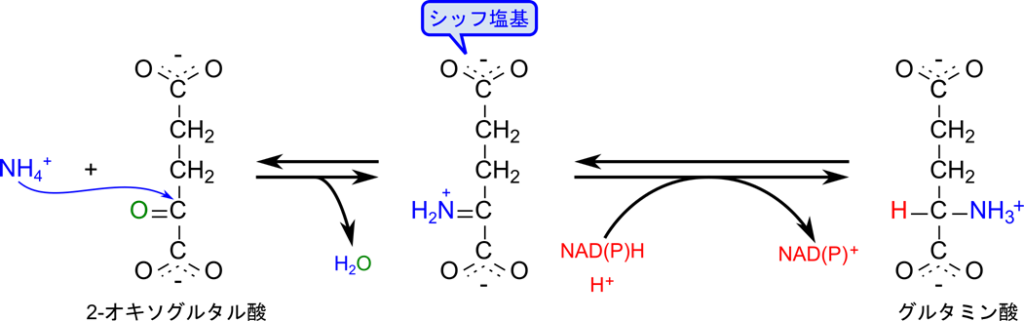
次にグルタミンの生合成について見ていきます。グルタミンの生合成ではグルタミン酸の側鎖カルボキシル基が ATP を消費してリン酸化されることで活性化されます。つまり、リン酸化されることでグルタミン酸は高エネルギー分子となり、アンモニウム塩の付加反応が起こりやすくなります。その後アンモニウム塩がエステル結合の炭素を求核的に攻撃して結合します。この時、リン酸基が遊離してグルタミンが生成されます(図3)。
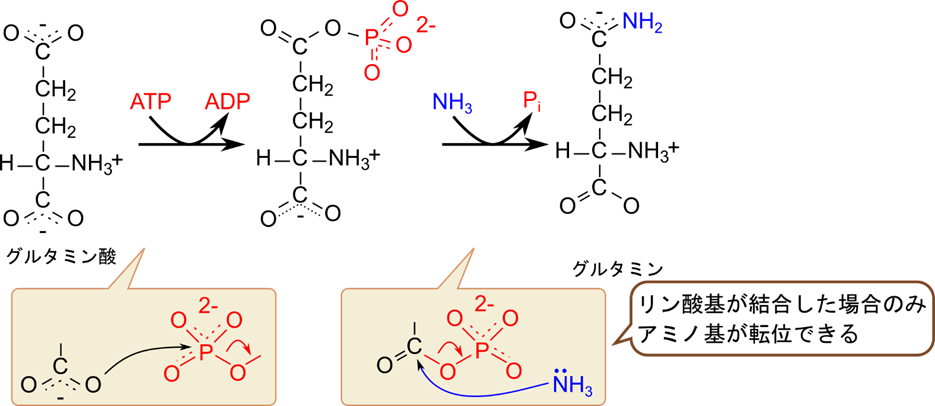
グルタミン酸とグルタミンの生合成には他のアミノ酸際立ってと異なる点があり、アミノ基の供給元はアンモニウム塩が利用されています。このため、これらの経路は単にアミノ酸の生合成経路というだけでなく、アミノ基の取り込みの意味も持っています。さらに、こうして得られたグルタミン酸とグルタミンは他のアミノ酸の生合成に当たりアミノ酸を供給するという役割も担っています。このように、アミノ基の取り込みと供給という観点で、これらの生合成経路はとても単純ですが、重要な意味を持っています。
プロリンとアルギニンの生合成経路
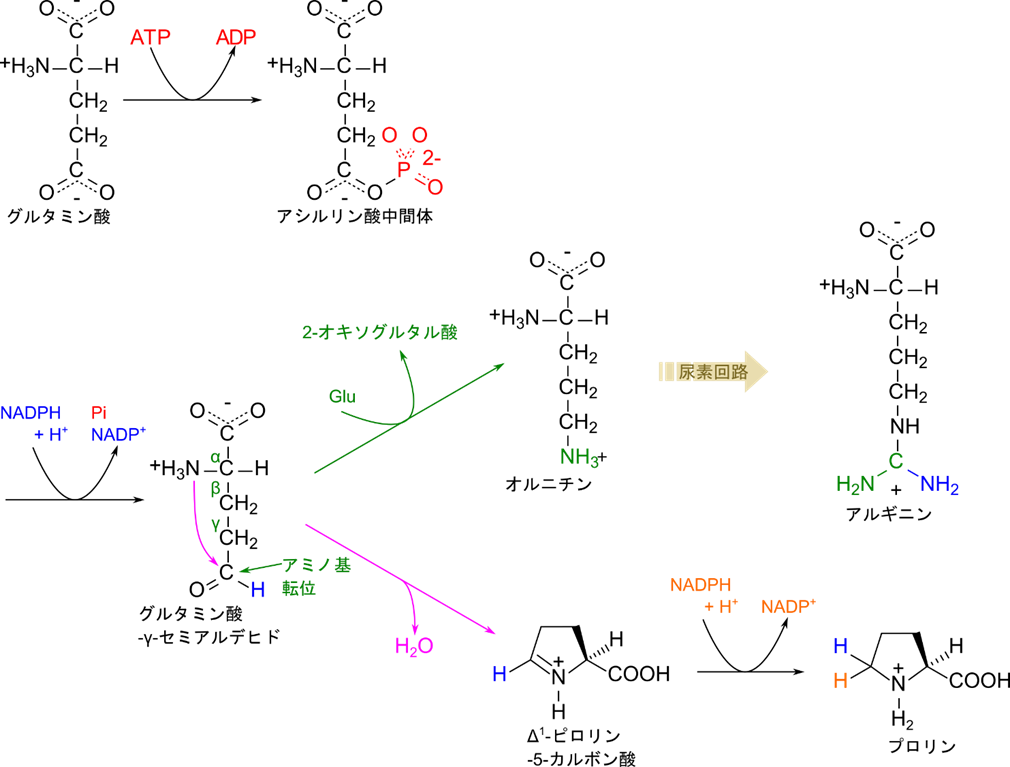
グルタミン酸の側鎖のカルボキシル基がアミノ基と結合して閉環するとプロリンの構造が与えられます。この反応経路ではまず、グルタミン酸が ATP を消費してリン酸化されることでアシルリン酸が生成されるます。グルタミン酸はリン酸化を受けることで高エネルギー分子となり、グルタミン酸-γ-セミアルデヒドへの変換をスムーズに行えるようにします。その後、同じ分子上のアミノ基がホルミル基の炭素原子を求核的に攻撃して結合し、閉環するとともに水分子が脱離します。さらに、生成されたΔ1-ピロリン-5-カルボン酸は還元されてプロトン化されるとプロリンが生成されます(図4)。
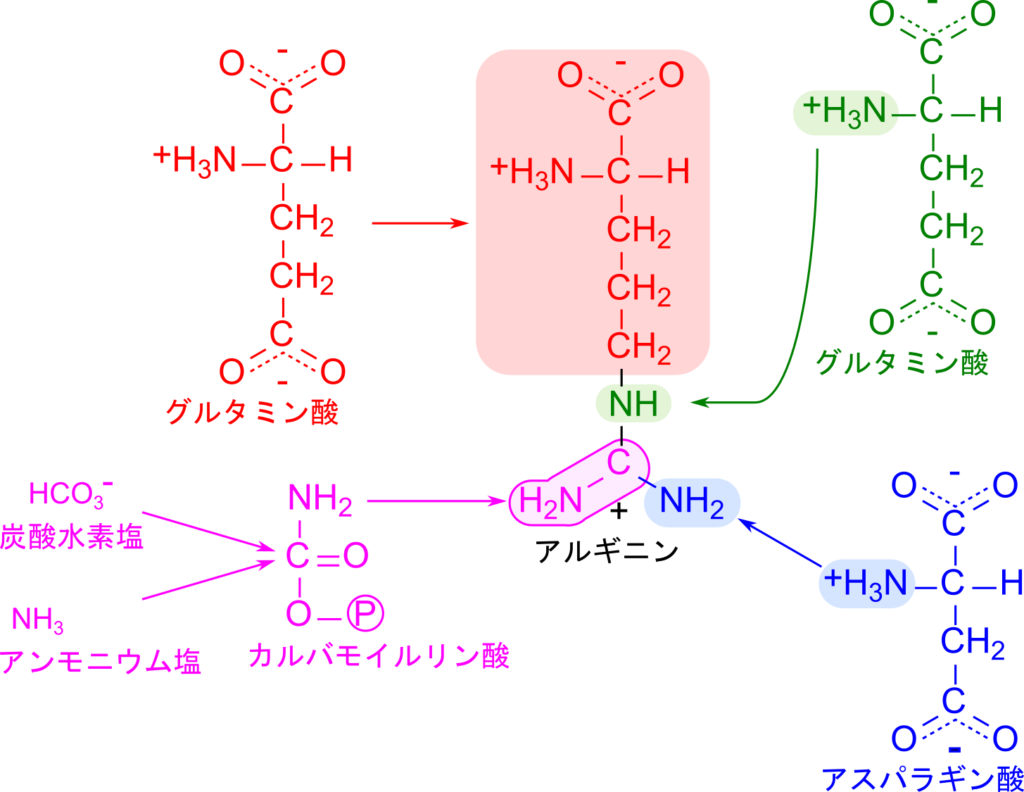
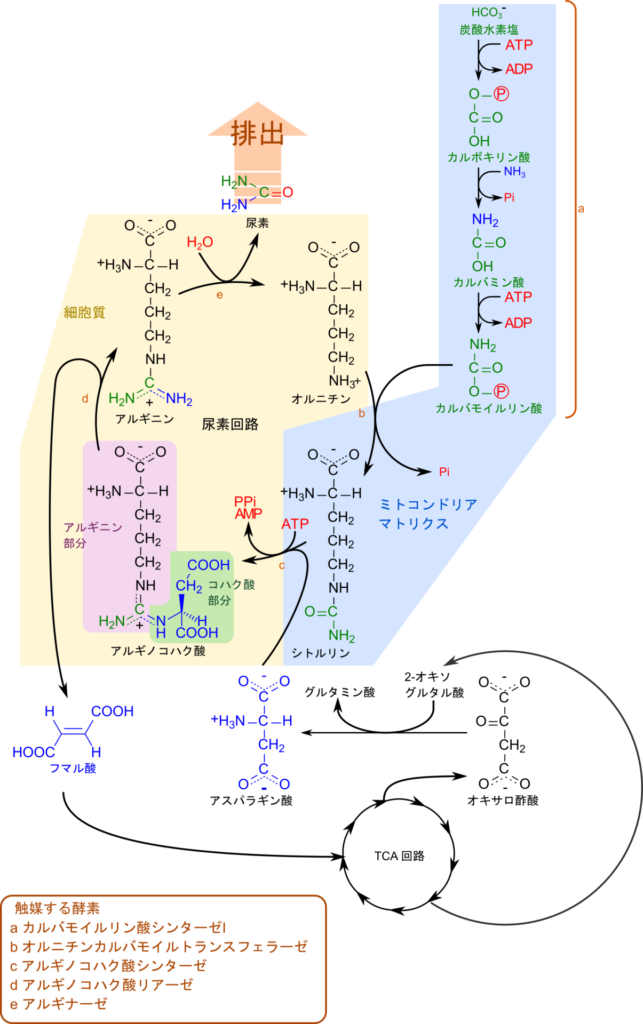
一方で、アルギニンの生合成は少し複雑です。そこで、アルギニンの各原子がどの分子に由来するのかを見ていきましょう(図3)。アルギニンの基本骨格はグルタミン酸によって供給されます。三つの窒素原子の内、δ炭素につながる窒素原子はグルタミン酸から供給され、末端の二つのアミノ基の内一つはアスパラギン酸から、残る炭素とアミノ基はカルバモイルリン酸から供給されます。ただし、カルバモイルリン酸は炭酸とアンモニウム塩から合成されますから、これらの炭素とアミノ基は炭酸とアンモニウム塩から供給されることになります。以上の内容を踏まえてアルギニンの生合成経路についてみていきましょう。
アルギニンの生合成ではプロリンの生合成と同様、グルタミン酸がアシルリン酸中間体を介して還元され、グルタミン酸-γ-セミアルデヒドが生成されることで始まります。その後、ホルミル基(-CHO基)がアミノ基転位を受けることでオルニチンが生成されます。この段階でアルギニンの δ 炭素に結合している窒素原子が導入されます。オルニチンはアンモニアの無毒化回路である尿素回路の中間体であり、生成されたオルニチンは尿素回路に合流します。尿素回路では炭酸塩とアンモニアから合成されたカルバモイルリン酸をオルニチンが受け取り、シトルリンに変換されます。この反応はカルバモイルリン酸のカルボニル基(C=O基)をアミノ基が求核的に攻撃して結合し、カルバモイルリン酸からリン酸基が脱離します。この過程では、側鎖末端の炭素と二つあるアミノ基のうち一つが導入されます。次いで、シトルリンがアスパラギン酸と結合し、アルギニノコハク酸(アルギニン+コハク酸の命名)を生成します。この反応は ATP を消費して、ピロリン酸(PPi)と AMP を生成します。ピロリン酸はさらに加水分解を受けて無機リン酸へと分解されます。このことにより、ATP 二分子に相当するエネルギーを得ることができ、反応を有利に進めることができます。ATP からピロリン酸を産生し、ピロリン酸の加水分解によりさらにエネルギーを得ることで反応を有利に進めるメカニズムはアスパラギン酸からアスパラギンを産生するときなど他の反応でもよくみられるメカニズムです(詳細はこちら)。この過程で、側鎖末端のアミノ基が導入されますが、コハク酸部分が余分ですので、フマル酸として脱離させてアルギニンが生成されます。
ここで、アルギニンの生合成が尿素回路に関連している点に注意してください。カルバモイルリン酸はアンモニアと炭酸から生成される分子であり、アルギニンはカルバモイルリン酸から窒素を供給されます。この過程は一見するとアンモニアの取り込みにアルギニンが関与しているように見えますが、アルギニンが生成される過程は窒素原子の排泄にかかわる経路です。つまり、アルギニンは窒素原子の排泄の過程の中間体ですので、アルギニンはアンモニアの取り込み関与しているのではなく、アンモニアの排泄に関与していると解釈されます。このように、同じくアンモニア由来のアミノ基が関与する反応であっても、グルタミン酸やグルタミンのようにアンモニアを取り込む反応と、(カルバモイルリン酸を介する間接的な過程ですが)アルギニンのようにアンモニアを排泄する反応では、生物学的な意味が大きく異なります。こうした違いは、反応がどのような経路の中で行われているかに注目することで理解が深まります。反応単体に着目するだけでなく、経路全体の意味を意識して学ぶことが重要です。
尿素回路について
尿素回路はアミノ酸の分解の結果生じたアンモニアを無毒化する経路です。詳しくはまたの機会に解説しようと思いますが、ここでは簡単に概説しようと思います。アミノ酸が分解されるとアンモニアが産生されますが、アンモニアは毒性が高いため、より毒性の低い尿素へ変換する必要があります。この過程は肝臓で行われ、尿素は腎臓を経て尿中に排泄されます。尿素回路は窒素の排泄に関与する回路とされますが、前述のように、中間体にアルギニンを持つことからアルギニンの生合成にも関与しています。尿素回路ではオルニチンからシトルリン、アルギニノコハク酸を経てアルギニンが生成されます。生成されたアルギニンから、尿素が遊離するとオルニチンが生成され、回路が完成します。つまり、生成されたアルギニンが利用されるとアルギニンの供給源となりますし、アルギニンから尿素が遊離してオルニチンに変換されると窒素の排泄にかかわる経路とみなすことができます。
なお、尿素回路にはアスパラギン酸を必要としますが、このアスパラギン酸は TCA 回路のオキサロ酢酸から生成されます。さらに、途中で遊離するフマル酸は TCA 回路の中間体であり、TCA 回路に合流していきます。このように尿素回路は TCA 回路と深く関連している経路でもあります。
Δ1-ピロリン-5-カルボン酸の命名法について
この命名法は少し珍しい表現ですし、複雑な命名になっているので読み解きにくいかもしれません。”Δ” を使った命名はたまに見かけることがありますので少し説明しようと思います。
まず、基本骨格についてみていきましょう。この化合物の基本骨格は五員環部分です。この部分はピロリン(pyrroline)と呼ばれる構造です(今回の場合は 1-ピロリンの構造と一致しています)。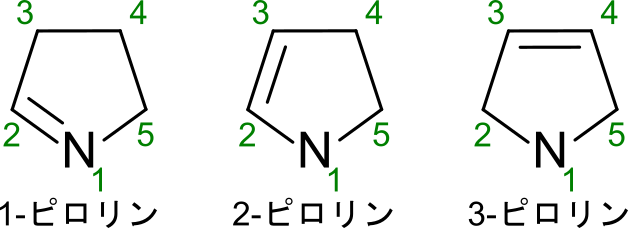
さらに、番号を付けていきます。ピロリンの場合、窒素を1番として二重結合のある方向に番号を振っていきます。なお、この時の二重結合の位置はΔを付けて表します。二重結合は 1 位と 2 位の炭素の間にありますが、この時は若いほうの番号使って表します。さらに二重結合は Double Bond の “D” のギリシャ文字 “Δ” を使ってを表します。したがって、今回の場合は “Δ1-” と表記されます。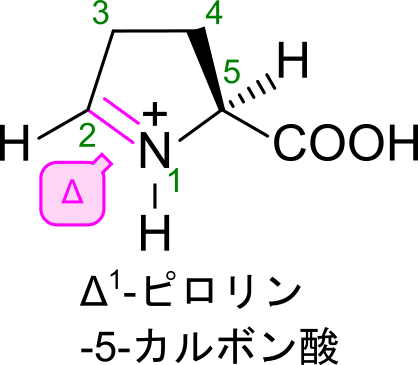
次に、置換基がどの位置についているのかを確認しましょう。今回はカルボキシル基が 5 位の炭素に結合しています。ですので、”5-カルボン酸” と表記されます。
以上の内容をまとめると、
Δ1:1-2 位に二重結合
5-カルボン酸:5 位の炭素にカルボキシル基が結合しているカルボン酸
となり、命名は
Δ1-ピロリン-5-カルボン酸
となります。
今回の記事では、2-オキソグルタル酸に由来するアミノ酸の生合成経路を紹介しました。グルタミン酸やグルタミンのようにアミノ基の取り込み・供給に関与するものから、環状構造を持つプロリン、さらには多数の窒素原子を含むグアニジノ基を持つアルギニンまで、特徴的なアミノ酸が含まれています。特にアルギニンの生合成は、アミノ酸の生合成経路でありながら尿素回路という分解・排泄系とも深く関わる、非常にユニークな経路です。こうした多様で興味深い生合成経路について、できるだけわかりやすく解説しました。ぜひ繰り返し読み返して、理解を深めてみてください。
参考文献
- 島原健三 (1991). 概説 生物化学. 三共出版. pp. 208-223
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp.665-693
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp.496-503
- KEGG PATHWAY DATABASE. 2025-03-03. https://www.genome.jp/kegg/pathway.html