脂肪酸は脂質の生合成に利用され、細胞の構造を支えたり、シグナル伝達を担ったりするなど、きわめて幅広い生体機能を支えています。この多様な役割は、脂肪酸を石油にたとえて考えると理解しやすいかもしれません。
脂肪酸がトリアシルグリセロールに取り込まれると、ガソリンや灯油のようにエネルギーを蓄える保管燃料としての役割を担います。一方で、リン脂質は細胞膜の主要な構成成分であり、建材のように細胞の構造を形づくるために利用されます。また、スフィンゴ糖脂質は細胞表面での認識や相互作用に関与することから、細胞の身分を示すIDカードのような役割を果たしています。さらに、エイコサノイド(アラキドン酸から生成される一群のシグナル伝達物質)は、免疫応答や発熱、血管拡張などの緊急性の高い生体反応を媒介しており、異常事態を知らせる警報器やパトランプに相当する機能を担っています。
この記事では、このように多様な場面で機能する脂質が、どのように合成されるのかについて紹介します。
Contents
グリセロ脂質とスフィンゴ脂質
脂肪酸はトリアシルグリセロールの前駆体となるだけでなく、様々な脂質の前駆体となります。その中でも生体膜を構成する脂質やシグナル伝達に関与する脂質の多くは、グリセロ脂質およびスフィンゴ脂質に分類されます。
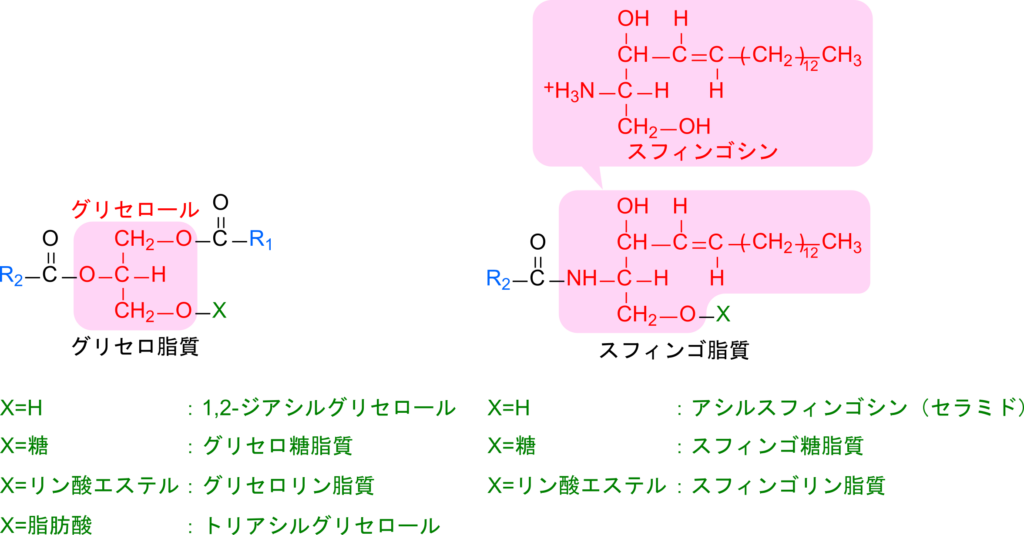
グリセロ脂質はグリセロールを基本骨格として1位、2位にアシル基が結合し、3位に様々な置換基が結合しています。図1にグリセロ脂質の構造と代表的な脂質を示しています。Xが水素原子の場合、1,2-ジアシルグリセロールであり、糖が結合した場合はグリセロ糖脂質、リン酸エステルが結合した場合はグリセロリン脂質、脂肪酸の場合にはトリアシルグリセロールと呼ばれます。
スフィンゴ脂質の場合にはスフィンゴシンが基本骨格となり、2位にアシル基が結合しています。Xが様々な置換基になり、置換基によって名称が変わります。Xが水素原子の場合にはアシルスフィンゴシン(セラミド)、糖の場合にはスフィンゴ糖脂質、リン酸エステルの場合にはスフィンゴリン脂質と呼ばれます。
今回の記事ではグリセロ脂質とスフィンゴ脂質の生合成について解説していきます。
エネルギーの貯蔵体、トリアシルグリセロールの合成
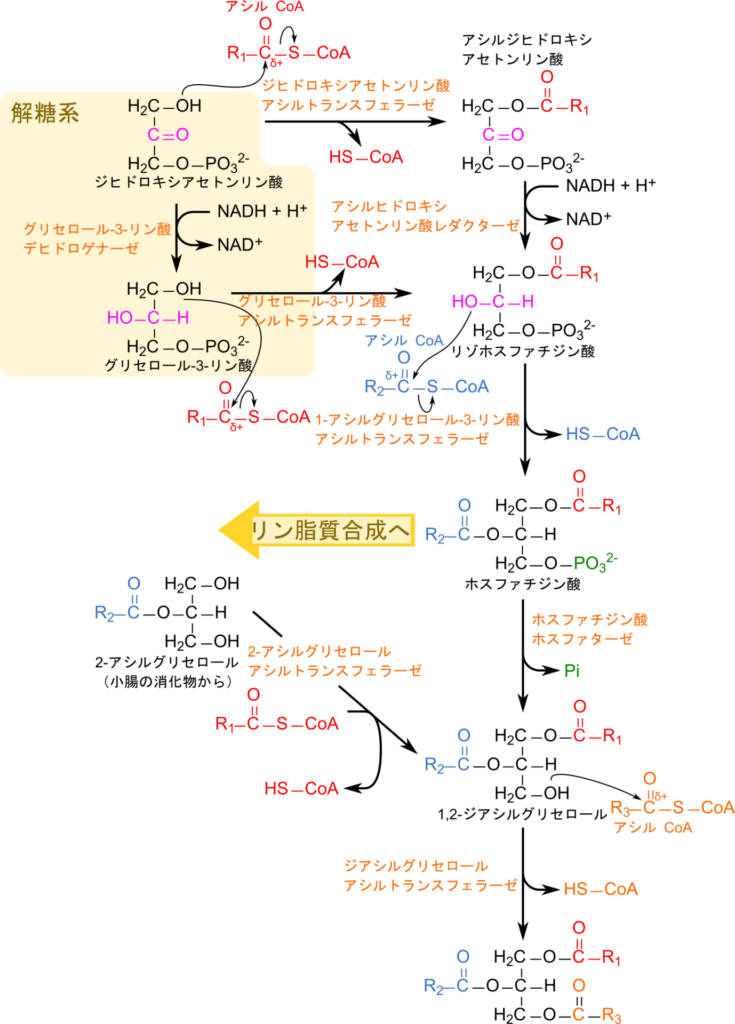
脂肪酸合成で合成された脂肪酸はグリセロール-3-リン酸またはジヒドロキシアセトンリン酸とともにトリアシルグリセロールの合成に利用されます(図2)。グリセロール-3-リン酸やジヒドロキシアセトンリン酸は解糖系や糖新生から供給されます。グリセロール-3-リン酸はグリセロール-3-リン酸デヒドロゲナーゼの作用によりジヒドロキシアセトンリン酸が還元されて供給されます。合成された脂肪酸はアシルCoA として供給され、アシル基転移反応によりアシルジヒドロキシアセトンリン酸が生成されます。生成されたアシルジヒドロキシアセトンリン酸が還元されるとリゾホスファチジン酸が生成されます。リゾホスファチジン酸の生成はグリセロール-3-リン酸からも生成されますが、この反応はグリセロール-3-リン酸アシルトランスフェラーゼが触媒します。リゾホスファチジン酸のグリセロール部分の2位の水酸基が1-アシルグリセロール-3-リン酸アシルトランスフェラーゼの作用により、ホスファチジン酸が生成されます。ホスファチジン酸はトリアシルグリセロールの原料となりますが、その一方でリン脂質の原料としても利用され、この点でホスファチジン酸はトリアシルグリセロール合成とリン脂質合成の結節点となります。ホスファチジン酸ホスファターゼの作用により、リン酸基が脱離して1,2-ジアシルグリセロールが生成されます。一方で小腸から吸収された2-アシルグリセロールに2-アシルグリセロールアシルトランスフェラーゼが作用して1位の水酸基にアシル基が転移されても1,2-ジアシルグリセロールが生成されます。こうして生成された1,2-ジアシルグリセロールは、ジアシルグリセロールアシルトランスフェラーゼの作用によりアシルCoA からアシル基が転移されてトリアシルグリセロールが生成されます。この過程で起こるアシル基転移反応は水酸基のカルボニル炭素への求核攻撃による反応として理解できます。
こうして生成されるトリアシルグリセロールは主に肝臓で生成されますが、その後VLDL を介して輸送され、筋肉でエネルギー源として利用されたり、脂肪細胞で貯蔵されます。
リン脂質の合成経路
ホスファチジルエタノールアミン、ホスファチジルコリン、ホスファチジルセリンの生合成
グリセロ脂質には前項で紹介したトリアシルグリセロールのほかに、ホスファチジルセリンやホスファチジルコリン、ホスファチジルグリセロールに代表されるリン脂質も知られています。ここではこれらリン脂質の合成経路についてみていきましょう。
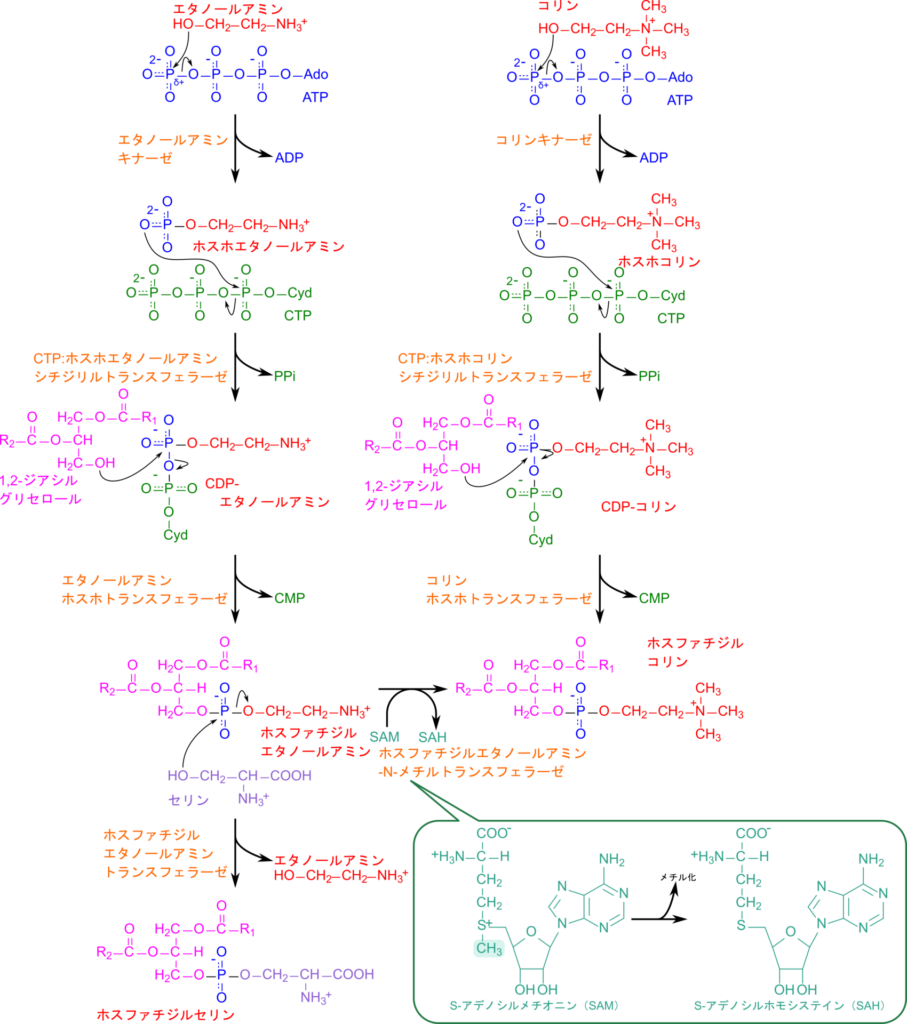
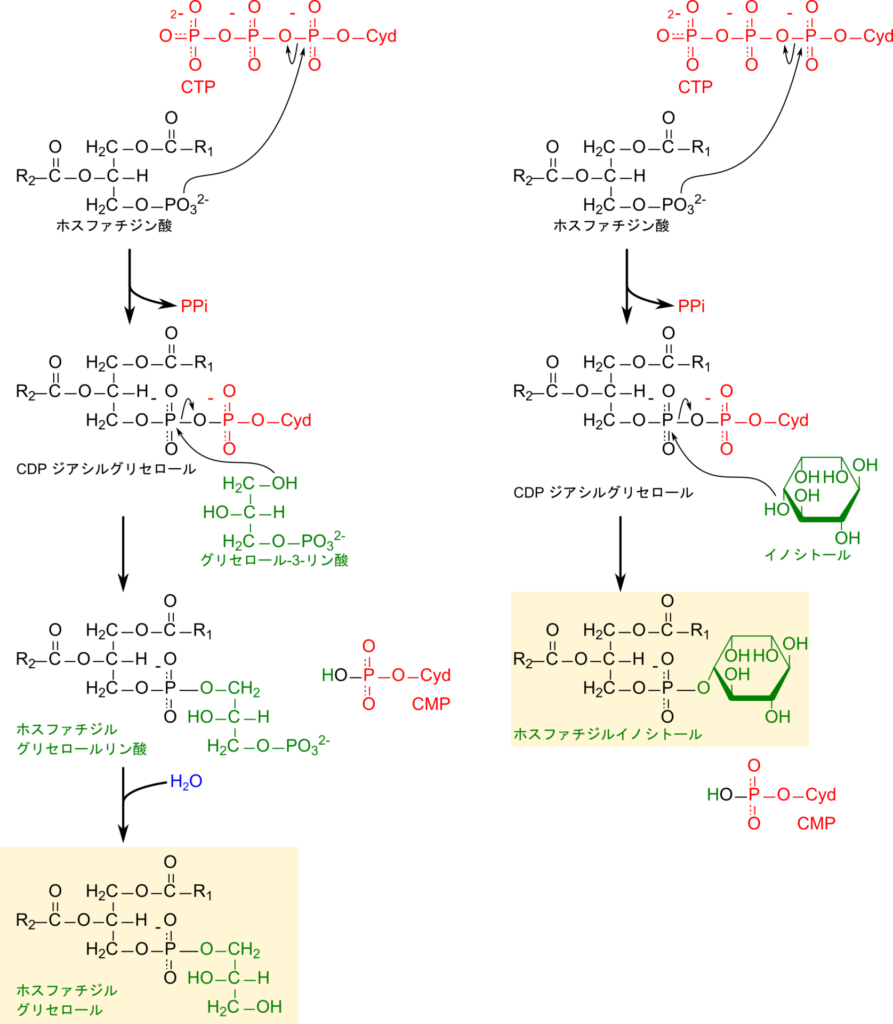
エタノールアミンはATP を消費してリン酸化され、ホスホエタノールアミンが生成されます。この反応を触媒する酵素はエタノールアミンキナーゼです。ホスホエタノールアミンのリン酸基の酸素原子がCTPのα-リン酸基を求核攻撃してピロリン酸が遊離し、CMPが転移されるとCDP-エタノールアミンが生成されます(この時CDPのリン酸基の内一つはホスホエタノールアミンに由来します)。この反応を触媒する酵素はCTP-ホスホエタノールアミンシチジルトランスフェラーゼです。こうして生成されたCDP-エタノールアミンは1,2-ジアシルグリセロールの水酸基の酸素原子がリン酸基を求核攻撃して結合し、エタノールアミンが1,2-ジアシルグリセロールに転移されてCMPが遊離し、ホスファチジルエタノールアミンが生成されます(図3)。
同様の反応によってホスファチジルコリンが生成されます。コリンがATPを消費してリン酸化されるとホスホコリンが生成されます。この反応はコリンキナーゼによって触媒されます。さらにホスホコリンのリン酸基の酸素原子がCTPのα-リン酸基を求核攻撃してピロリン酸が遊離し、CMPが転移されるとCDP-コリンが生成されます(この時CDPのリン酸基の内一つはホスホコリンに由来します)。CDP-コリンのリン酸基が1,2-ジアシルグリセロールの水酸基の酸素原子によって求核攻撃され転移されるとCMPを遊離してホスファチジルコリンが生成されます。
なお、ホスファチジルエタノールアミンはホスファチジルエタノールアミン-N-メチルトランスフェラーゼが作用してS-アデノシルメチオニン(SAM)によりメチル化されるとホスファチジルコリンに変換されます。SAMは代表的なメチル基供与体でDNAやRNAのメチル化やタンパク質のメチル化に関与する物質です(詳しくはこちら)。
ホスファチジルエタノールアミンはホスファチジルエタノールアミントランスフェラーゼの作用によりエタノールアミンがセリンと交換されてホスファチジルセリンが生成されます。これらの分子はいずれもアシル基の無極性部位とエタノールアミン・セリン・コリンの極性部位を持つ両親媒性の分子であり、膜脂質として重要な分子です。
ホスファチジルグリセロールとホスファチジルイノシトールの生合成
ホスファチジン酸はホスファチジルグリセロールやホスファチジルイノシトールの前駆体にもなります。
ホスファチジン酸のリン酸基の酸素原子がCTPのα-リン酸基を求核的に攻撃してピロリン酸を遊離させると CDP-ジアシルグリセロールとなって活性化されます。ホスファチジルグリセロールの生合成ではグリセロール-3-リン酸の1位の水酸基の酸素原子がCDP-ジアシルグリセロールのリン酸基を求核攻撃して結合しCMPが遊離します。するとホスファチジルグリセロールリン酸が生成され、リン酸基が加水分解して遊離するとホスファチジルグリセロールが生成されます(図4)。
ホスファチジルイノシトールではグリセロール-3-リン酸の代わりにイノシトールの水酸基がCDP-ジアシルグリセロールのリン酸基を求核的に攻撃して結合し、CMPを遊離させてホスファチジルイノシトールを生成します(図4)。
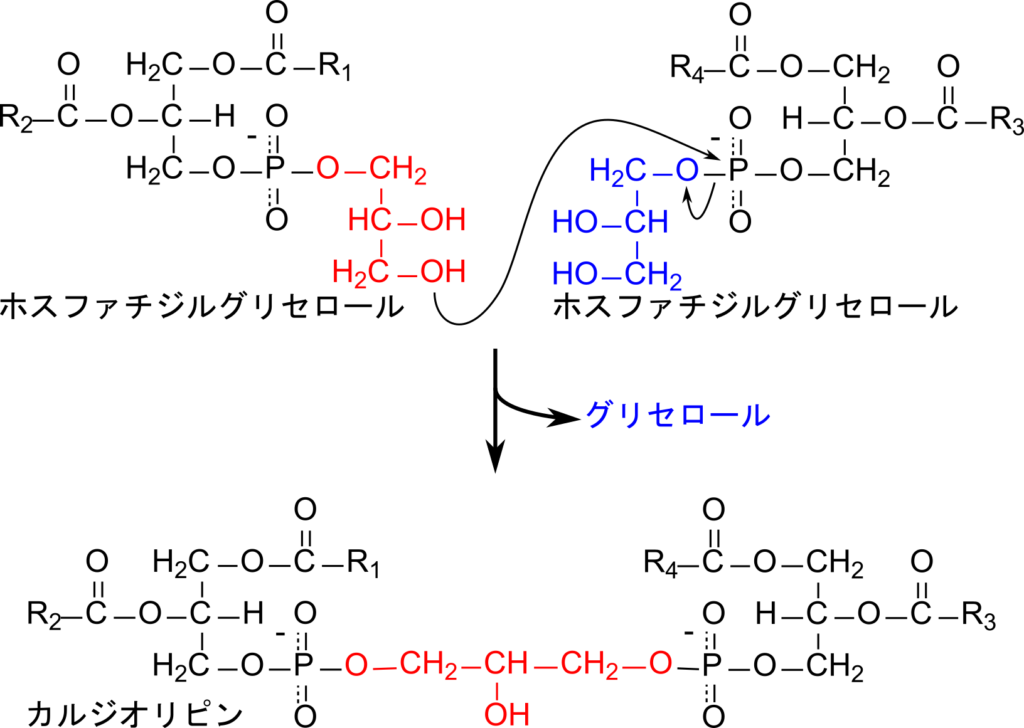
カルジオピンの生合成
カルジオピンの生合成はホスファチジルグリセロールに分子が会合することで生成されます。この反応では一方の末端の水酸基がもう一方の分子のリン酸基を求核的に攻撃してグリセロールが遊離することで生成されます(図5)。
スフィンゴ脂質の生合成
スフィンゴ脂質は真核細胞の細胞膜にみられ、特に中枢神経に高濃度に存在します。スフィンゴ脂質はグリセロ脂質と異なり、基本骨格はスフィンゴシンです。スフィンゴ脂質はセラミドから生成されます。この記事ではセラミド生成から初めてセレブロシドとスフィンゴミエリンの生合成について解説し、最後にガングリオシドの生合成について簡単に説明していきます。
セラミドの生合成
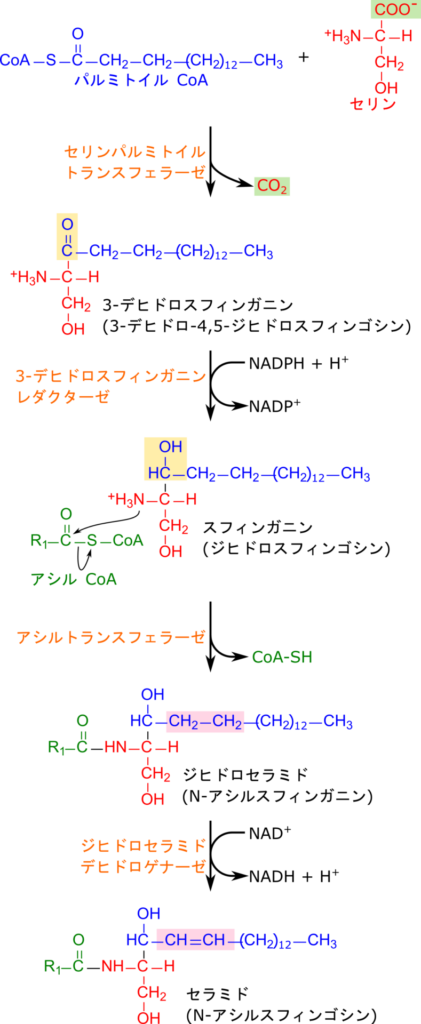
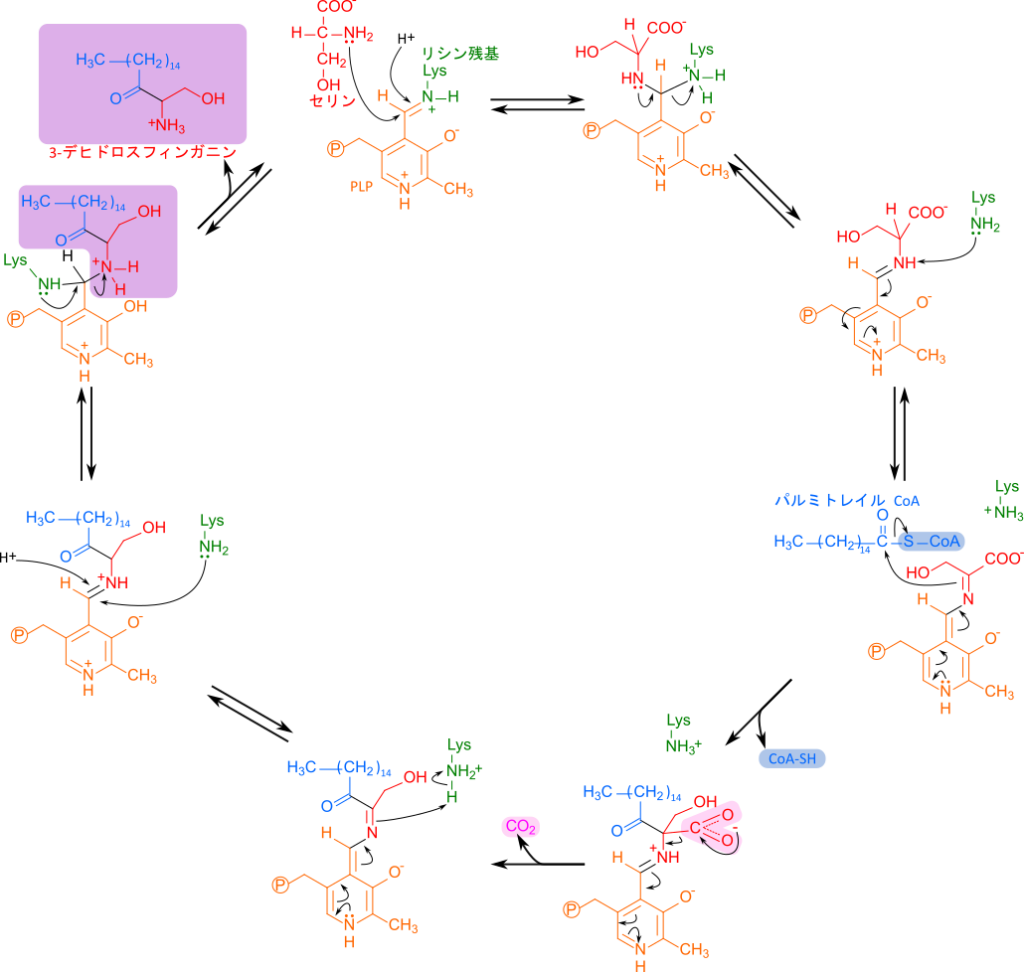
セラミドはパルミトイル CoA(パルミチン酸;C16 の脂肪酸+CoA)とセリンから生成されます。この反応はセリンパルミトイルトランスフェラーゼにより触媒され、ピリドキサールリン酸(PLP)を要求する反応です。セリンがリシンと入れ替わる形でPLPと結合してシッフ塩基を与えます。ここにパルミトイルCoAが供給されると PLP 上でセリンの炭素骨格とパルミトイル CoA の縮合が進み、さらにセリンのカルボキシル基が炭酸として遊離して最終的にリシン残基との再結合(内部アルジミン形成)を経て、3-デヒドロスフィンガニンが遊離します(図6、7)。その後3-デヒドロスフィンガニンが還元されてスフィンガニンが生成されます(3-デヒドロスフィンガニンレダクターゼ)。アシルトランスフェラーゼによりアシルCoAからアミノ基にアシル基が転移されるとジヒドロセラミドが生成され、ジヒドロセラミドデヒドロゲナーゼがジヒドロセラミドを酸化すると二重結合が導入されてセラミドが生成されます(図6)。
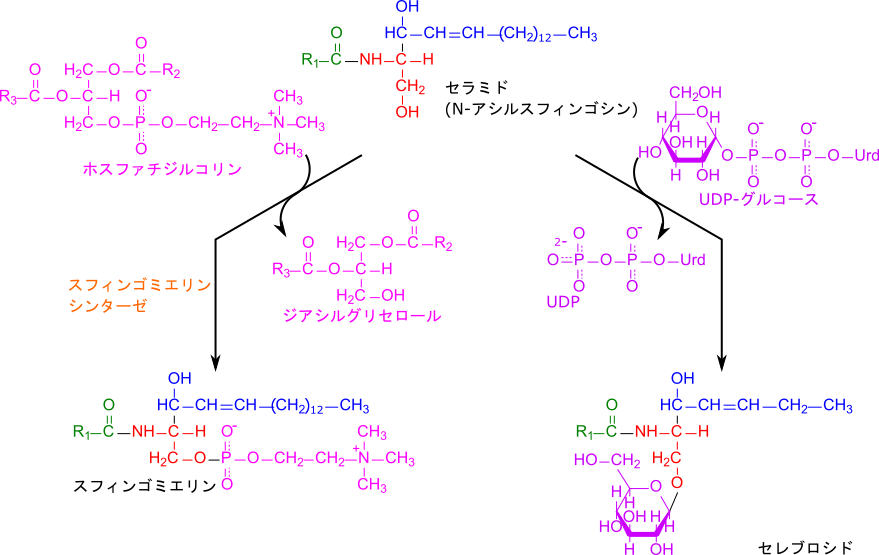
セラミドはさらにホスファチジルコリンからホスホコリン部分を受け取ってスフィンゴミエリンを生成します。スフィンゴミエリンは神経線維を覆うミエリン鞘を構成します。一方でUDP-グルコースやUDP-ガラクトースから糖を受け取ると糖脂質であるセレブロシドとなります(図8)。
スフィンゴ糖脂質の種類と生合成
スフィンゴ糖脂質はスフィンゴシンを基本骨格とし、様々な糖鎖が結合したものの総称です。特に、ガングリオシドはシアル酸を含むスフィンゴ糖脂質であり(図9)、神経系に豊富に存在する重要な糖脂質です。その種類は非常に多く、100種類以上が同定されています。
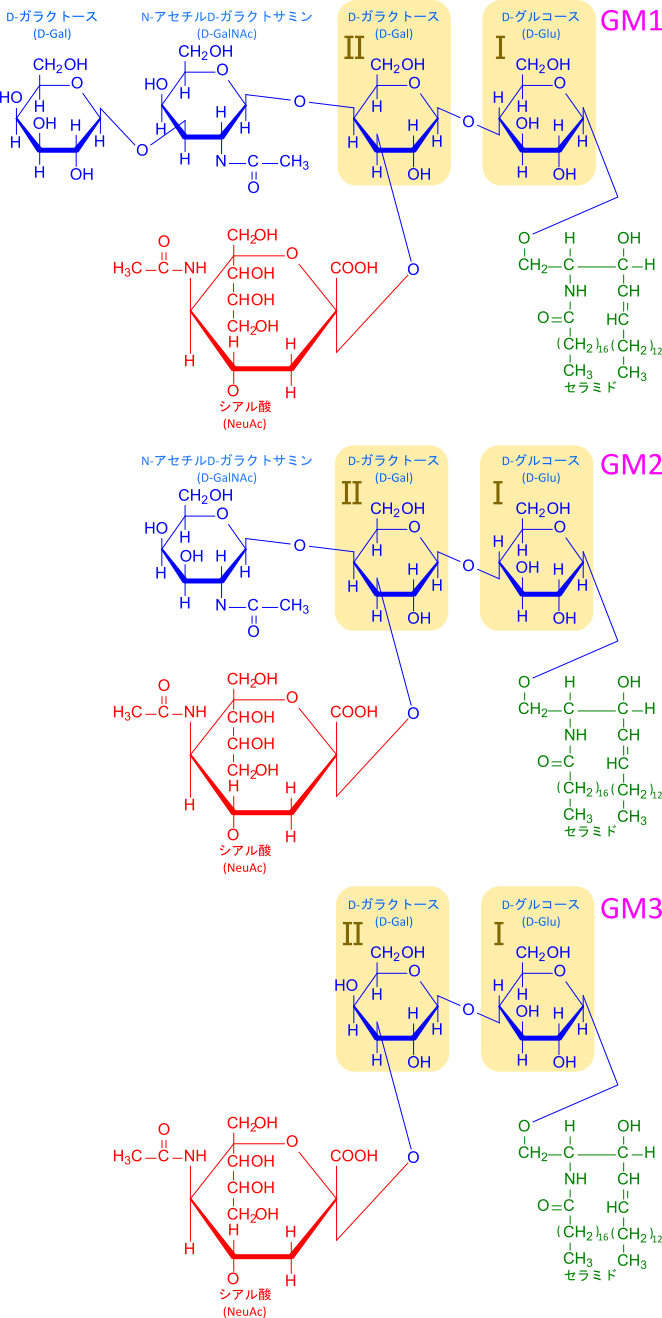
スフィンゴ糖脂質(糖鎖部分を持つスフィンゴ脂質)の分類を表1に示します。ガングリオシドを含むスフィンゴ糖脂質は糖鎖部分の配列パターンによっていくつかに分類されます。また、これらのスフィンゴ糖脂質は図9のⅡで示すD-ガラクトースに結合しているシアル酸の数によって以下のように分類されます。
- 0個:asialo series(アシアロ系列)
- 1個:a series(a系列)
- 2個:b series(b系列)
- 3個:c series(c系列)
| 系列 | 基本的な構造 |
| Globo | GalNAcβ1, 3 Galα1, 4Galβ1, 4Glcβ1, 1 ‘Cer |
| Isoglobo | GalNAcβ1, 3 Galα1, 3 Galβ1, 4Glcβ1, 1 ‘Cer |
| Ganglio | Galβ1, 3 GalNAcβ1, 4Galβ1, 4Glcβ1, 1 ‘Cer |
| Isoganglio | Galβ1–3 GalNAcβ1–3 Galβ1–4Glcβ1–1’Cer |
| Lacto | Galβ1, 3 GlcNAcβ1, 3 Galβ1, 4Glcβ1, 1 ‘Cer |
| Neolacto | Galβ1, 4GlcNAcβ1, 3 Galβ1, 4Glcβ1, 1 ‘Cer |
| Lactoganglio | GalNAcβ1, 4(GlcNAcβ1, 3)Galβ1, 4Glcβ1, 1’Cer |
| Muco | Galβ1, 4Galβ1, 4Glcβ1, 1’Cer |
| Gala | Galα1, 4Galβ1, 1’Cer |
| Neogala | Galβ1, 6Galβ1, 6Galβ1, 1’Cer |
| Mollu | GlcNAcβ1, 2Manα1, 3Manβ1, 4Glcβ1, 1’Cer |
| Arthro | GalNAcβ1, 4GlcNAcβ1, 3Manβ1, 4Glcβ1, 1’Cer |
| Schisto | GalNAcβ1, 4Glcβ1, 1’Cer |
| Spirometo | Galβ1, 4Glcβ1, 3Galβ1, 1’Cer |
名称はスヴェンネルホルム(Svennerholm)の略号命名法が好んで使用され、IUPAC 命名法はあまり使用されない傾向にあるようです。この命名法では系列名(G:ガングリオシドとL:ラクトシルセラミドを含む系統など)、シアル酸の数(A=0, M=1, D=2, T=3, Q=4, P=5, H=6, S=7)が含まれます。また、名称の最後の番号は糖鎖の長さ順になっています。例えばGM1であれば中性糖の長さは(5-1=4)4個となります。GM4であれば同様に1つとなります。この時、シアル酸は酸性糖であり、この数には含みませんので注意してください。
これらのスフィンゴ糖脂質はセラミドにガラクトースやグルコース、N-アセチルガラクトサミンのような中性糖やシアル酸が付加されて生成されます。この時付加される糖はUDP-ガラクトースやUDP-グルコース、シアル酸の場合にはCMP-N-アセチルノイラミン酸(CMP-シアル酸)として活性化されたものが利用されます。
脂肪酸の不飽和化
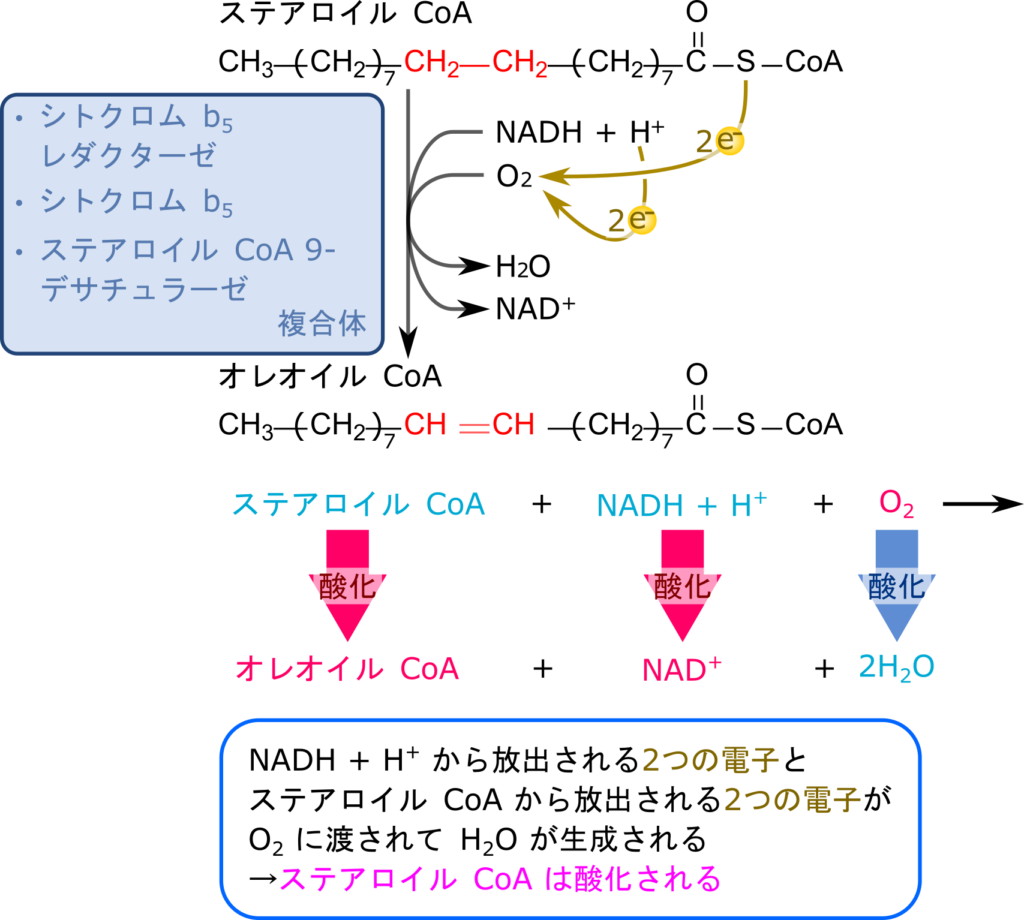
小胞体では長鎖アシルCoAに二重結合を導入することも行います。ここではステアロイルCoAを例に見ていきましょう。ステアロイルCoAの不飽和化はシトクロムb5レダクターゼ(cytochrome-b5 reductase)、シトクロムb5(cytochrome b5)、ステアロイルCoA 9-デサチュラーゼ(stearoyl-Coa 9-desaturase)の3種類の膜結合タンパク質が関与して行われます。この反応は以下のようにして起こります。
ステアロイルCoA(飽和)+NADH+H++O2→オレオイルCoA(不飽和)+NAD++H2O
この反応ではステアロイルCoAとNADHが酸化され、酸素が還元される反応です。
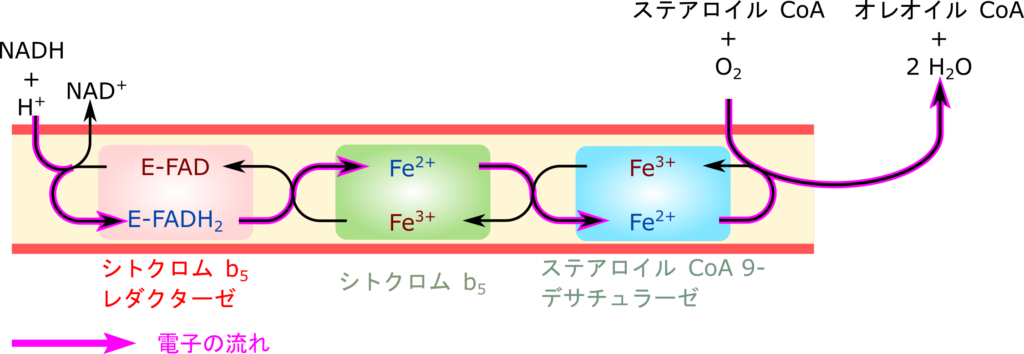
ステアロイルCoAの不飽和化についてより詳細を見ていきましょう。二重結合の導入はまずNADHがシトクロム b5 レダクターゼのFADへ電子を渡すことでFADH2が生成されます。生成されたFADH2はシトクロムb5のヘム鉄原子(Fe3+)に電子を渡してFe2+へ変換します。さらにステアロイルCoA 9-デサチュラーゼの非ヘム鉄原子(Fe3+)に電子を渡してFe2+へ変換し、最終的にこの鉄原子から酸素に電子を渡すとともにステアロイルCoA からも電子を抜き取って酸素に渡し、水を生成するとともにオレオイルCoAを生成します。
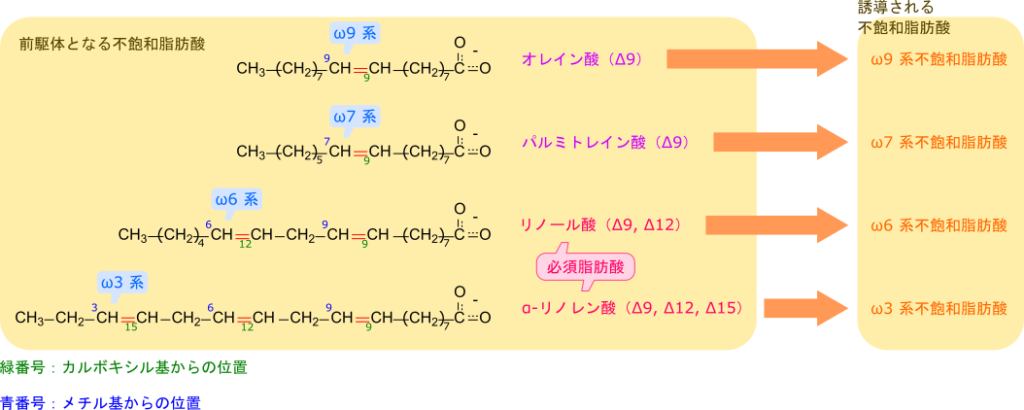
このようにして生成される不飽和脂肪酸は様々なものがありますが、ω末端(炭素鎖末端側)から数えて最初の二重結合までの炭素数によって前駆体となる不飽和脂肪酸がわかります。例えば炭素鎖末端から数えて9個目の炭素と10個目の炭素の間に二重結合がある不飽和脂肪酸はそれよりもカルボキシル末端側に二重結合が複数持っているような脂肪酸でもオレイン酸が前駆体となって合成されている脂肪酸であることがわかります。このことから、不飽和脂肪酸は炭素鎖末端側から最初の二重結合までの炭素数によって系統分けすることができ、ωx 系というように呼ばれます。例えばリノール酸の場合は炭素鎖末端側から6-7 個目と8-9 個目に二重結合がありますので、最初の二重結合の位置をとってω6系不飽和脂肪酸に分類されます。
エイコサノイドホルモンの合成
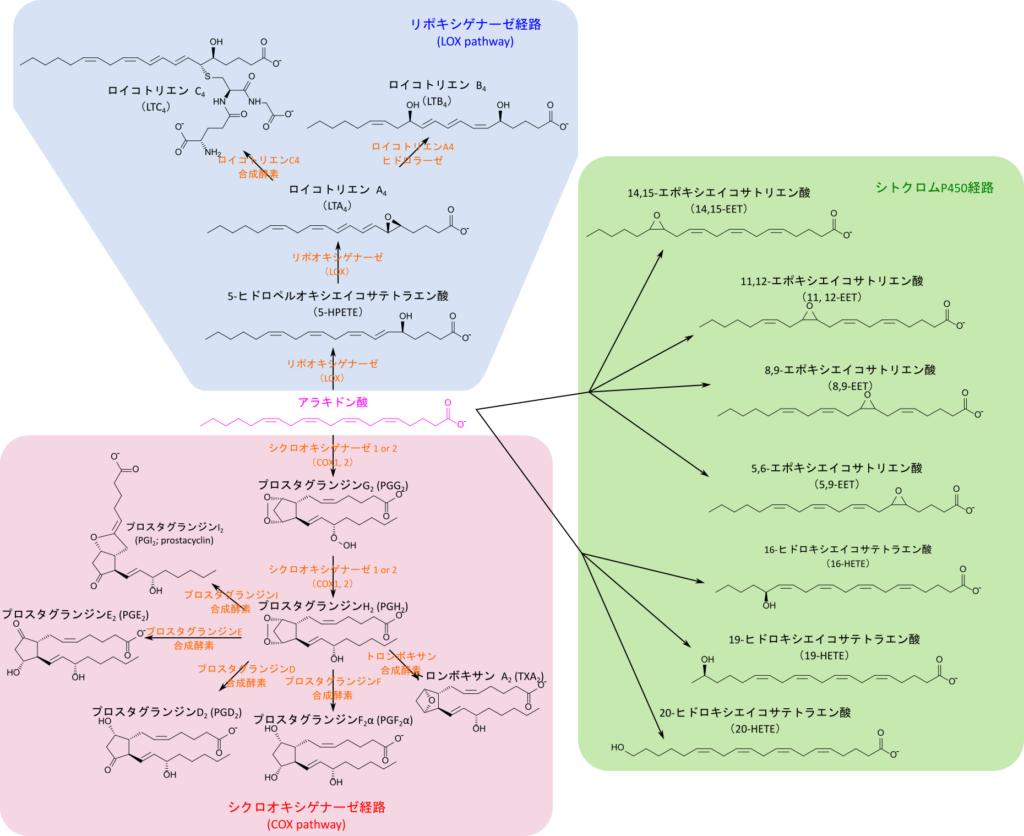
リノール酸から誘導されるアラキドン酸(arachidonate; 20:4 Δ5, Δ8, Δ11, Δ14)はプロスタグランジン、プロスタサイクリン、トロンボキサン、ロイコトリエンなどのシグナル伝達物質(エイコサノイドホルモン)の前駆体となります。アラキドン酸はω6系の脂肪酸で炭素数が20、二重結合が4つ含む脂肪酸です。これらのエイコサノイドホルモンの生合成経路はシクロオキシゲナーゼ(COX)経路、リポキシゲナーゼ(LOX)経路、シトクロムP450経路などが知られています(図13)。これらの経路で誘導される分子と機能を表2に示します。なお、各物質名の添え字(下付き数字)はその物質が持つ二重結合の数を表しています。
COX 経路ではCOX の作用によりプロスタグランジンG2、さらにH2 が生成されます。プロスタグランジンから各反応を通じてプロスタグランジンD2、E2、I2、F2α、トロンボキサンA2 などが誘導されます(図13)。
LOX 経路ではリポキシゲナーゼの作用により5-ヒドロペルオキシエイコサテトラエン酸(5-HPETE)、さらにロイコトリエンA4(LTA4)が生成されます。LTA4からはさらにロイコトリエンC4やB4が誘導されます(図13)。
シトクロムP450経路ではCYPエポキシゲナーゼによりエポキシエイコサトリエン酸(EET)が、ω-ヒドロキシラーゼによりヒドロキシエイコサテトラエン酸(HETE)が生成されます(図13)。
このように、アラキドン酸は複数の代謝経路を通じて多様な脂質性シグナル伝達物質へと変換され、生体内における炎症応答、血管機能、免疫調節などに重要な役割を果たしています。
| COX 経路 | |
| PGD₂ | 血小板凝集抑制に伴う発赤・腫脹を伴う血管拡張 肥満細胞成熟 アレルギー応答における好塩基球・好酸球の動員 |
| PGE₂ | TNF-α発現低下 マクロファージでIL-10増加 子宮収縮 血管拡張・発熱 好中球のエイコサノイド「クラススイッチング」 神経伝達物質放出増強 |
| PGI₂ | 血小板凝集抑制 IL-10上方制御、TNF-α下方制御 |
| PGF₂α | 血管収縮・気管支収縮 平滑筋・子宮収縮 |
| TXA₂ TXB₂ | 血小板凝集の調節 血管収縮・気管支収縮 |
| LOX 経路 | |
| LTB₄ | 好中球走化性、血管透過性、T細胞増殖 PPARαを介してLTB₄合成を負に制御(負のフィードバック) |
| LTC₄ LTD₄ LTE₄ | 炎症に応答して損傷部位へ白血球を動員 気管支収縮促進 喘息・アナフィラキシーに関与 気道・腸管で粘液分泌促進 |
| LXA₄ LXB₄ | 細菌排除促進 創傷治癒に関与するマクロファージの促進 貪食 死細胞除去(エフェロサイトーシス) |
| 8-HPETE 12-HPETE 15-HPETE | PPARに結合し炎症の恒常性維持に関与 肝臓でコレステロールレベルを調節 |
| CYP450 経路 | |
| EETs | 血管拡張 抗炎症作用および血管新生機能 Na⁺輸送の抑制 |
| HETE | 血管収縮 |
下の図を参照して、問1・問2に答えてください。
![脂質合成の問題図(中間体[1]〜[5]と酵素(a)〜(h))](https://www.lifescience-note.net/wp-content/uploads/2026/01/Lipid_synthesis_question.png)
問1.[1]~[5] に当てはまる分子を選べ
問2.(a)~(h) に当てはまる酵素名を選べ
下の図を参照して、問1・問2に答えてください。
![ホスファチジルエタノールアミン合成の問題図(中間体[1]〜[3]と酵素(a)〜(e))](https://www.lifescience-note.net/wp-content/uploads/2026/01/Lipid_synthesis_question2.png)
問1.[1]~[3] に当てはまる分子を選べ
問2.(a)~(e) に当てはまる酵素名を選べ
ホスファチジルグリセロールの生合成について正しい記述を選べ
スフィンゴ糖脂質に関する記述で正しいものを選べ
ステアリン酸の不飽和化に関する記述で正しいものを選べ
アラキドン酸から誘導されるシグナル伝達物質について正しい記述を選べ
参考文献
- 島原健三 (1991). 概説 生物化学. 三共出版. pp. 190-207
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp. 718-747
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp. 440-476
- Smith, S., & Tsai, S.-C. (2007). The type I fatty acid and polyketide synthases: a tale of two megasynthases. Natural Product Reports, 24(5), 1041–1072. https://doi.org/10.1039/b603600g
- Maier, T., Leibundgut, M., & Ban, N. (2008). The Crystal Structure of a Mammalian Fatty Acid Synthase. Science, 321(5894), 1315–1322. https://doi.org/10.1126/science.1161269
- UCHIYAMA, M. (1974). Biosynthesis and Organic Synthesis of Fatty Acids. Journal of Japan Oil Chemists’ Society, 23(10), 599–604. https://doi.org/10.5650/jos1956.23.599