セリンは 3-ホスホグリセリン酸から誘導され、グリシンとシステインの前駆体となります。これらの生合成経路は一見シンプルに見えますが、その過程で生じる副産物には様々な生合成経路で重要な役割を担う物質を含みます。本記事では、セリン・グリシン・システインの合成経路だけでなく、それらの持つ多機能性についても詳しく紹介します。
Contents
セリン、システイン、グリシンの生合成経路
3-ホスホグリセリン酸は解糖系の中間体ですが、セリン生合成の前駆体ともなります。さらに、セリンはグリシンやシステインの前駆体となります(図1)。
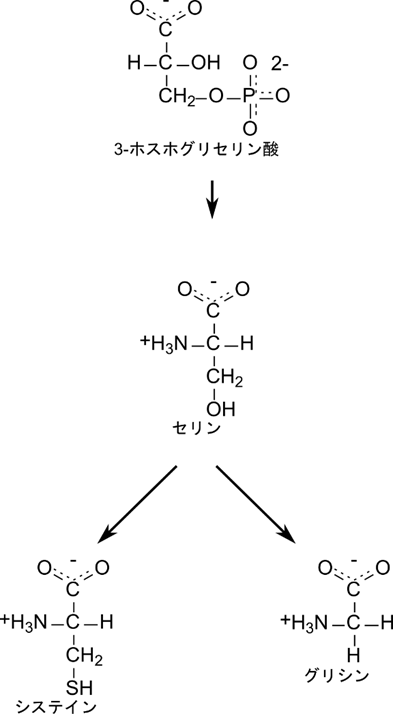
セリンの生合成経路
まずは 3-ホスホグリセリン酸からセリンの生成についてみていきましょう。この過程は比較的単純で、3-ホスホグリセリン酸にアミノ基を導入すれば、セリンとなります。ただし、3-ホスホグリセリン酸のままではアミノ基を転移させられません。そこで、一度ケトンに変換してから生合成経路を進めます。詳細をみていきましょう。3-ホスホグリセリン酸が酸化されることで 3-ホスホヒドロキシピルビン酸に変換されます。グリセリン酸(CH2(OH)-CH(OH)-COOH)の構造がピルビン酸(CH3–CO-COOH)の構造に変換されている点に注目してください。この反応はアルコールの酸化によるケトンの生成です。ピルビン酸は 2-オキソ酸でもありますので、アミノ基転位を受けることができます。ケト基にアミノ基が転位されると 3-ホスホセリンになります。最後に、加水分解によりリン酸基が遊離するとセリンが生成されます。こうして生成されたセリンはシステインやグリシンの前駆体となります。

システインの生合成とメチオニンの異化、活性型メチル基回路とメチル化
システインの生合成とメチオニンの異化経路
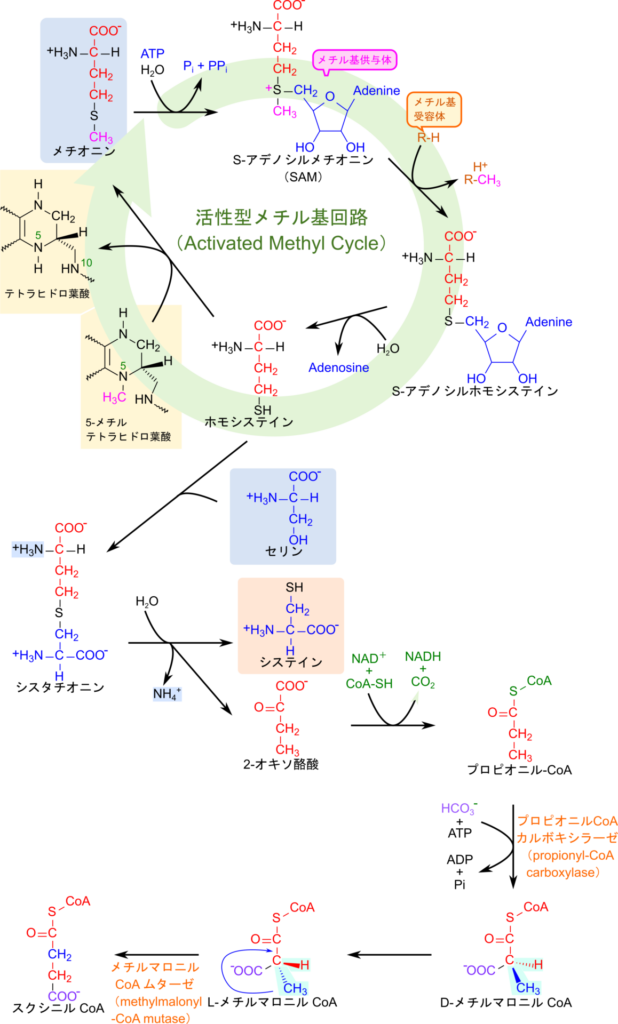
次に、システインの生合成経路についてみていきましょう。システインの生合成経路はメチオニンの分解と深く関連しており、メチオニンは分解される過程で硫黄をセリンに渡してシステインを生成します。このことから、今回の記事ではメチオニンを出発点として説明します。最初はメチオニンが ATP と反応してアデノシンと会合し、 S-アデノシルメチオニン(S-adenosylmethionine; SAM)を生成します。この反応は珍しい反応で、ATP の三つのリン酸基はリン酸基(Pi)とピロリン酸(PPi)を遊離します。なお、遊離したピロリン酸はすぐに分解され無機リン酸(Pi)にされます。この時産生された SAM は代表的なメチル基供与体で、メチル基を様々な分子に付加する性質を持っています。SAM はメチル基を転位する能力がかなり高く、硫黄に結合しているメチル基を様々な分子に渡して、S-アデノシルホモシステインに変換されます。その後、アデノシンが遊離するとホモシステインが生成されます。ホモシステインのチオール基(-SH 基)とセリンの水酸基で脱水縮合するとシスタチオニンとなります。この時点でメチオニンの硫黄がセリンに導入されます。最後にシスタチオニンから脱アミノ化されるとともに 2-オキソ酢酸が遊離するとシステインが生成されます。なお、遊離した 2-オキソ酢酸は CoA が導入され、脱炭酸、異性化を経てスクシニル CoA に変換され、TCA 回路に合流していきます。
SAM(S-アデノシルメチオニン)の役割
ここで、重要な中間体である SAM について解説します。メチオニンとアデノシンが会合すると、硫黄原子にメチレン基が配位するため硫黄原子が正電荷をもつようになります。この正電荷を持った硫黄原子が重要で、硫黄原子がメチル基の電子を強く引き込むことで(メチル基周りの電子密度が低下するため)メチル基の求電子性が高まります。求電子性が高まったメチル基は窒素原子や酸素原子、硫黄原子などの求核剤の攻撃を受けやすくなり、その結果メチル基の転位ポテンシャルが高くなります(メチル基を転位しやすくなります)。このように、メチオニンと ATP の反応では、よく見かけるリン酸化ではなく、アデノシンが会合するという不思議な反応経路を経て進みますが、このことで、SAM という重要なメチル基供与体を得ることができるのです。SAM は様々な分子をメチル化することで知られており、DNA や RNA のような核酸やタンパク質、脂質など実に多様な分子をメチル化します。
メチル化には様々な意味があります。いくつかの例を紹介しましょう。細菌ではファージなどから身を守るため DNA を切断する制限酵素を持っていますが、自分の制限酵素で自身の DNA が切断されてしまうと不都合になります。そこで、細菌は DNA をメチル化することで制限酵素の活性から自身のDNAを保護しています。他にも、mRNA の5′ 末端をメチル化することで mRNA を保護したり(キャップ構造)、ホスファチジルエタノールアミンをメチル化することで代表的なリン資質であるホスファチジルコリンを生成するなど、メチル化は生体内で様々な役割を担っています。
活性型メチル基回路
メチル基を転位した後 S-アデノシルメチオニン(SAM)は S-アデノシルホモシステインとなり、その後、ホモシステインが生成されます。ホモシステインがセリンと会合するとシステインの生成とメチオニンの異化経路に向かいますが、一方で、5-メチルテトラヒドロ葉酸からメチル基を受け取ると、メチオニンが再生されます。するとメチオニン→SAM→S-アデノシルホモシステイン→ホモシステイン→メチオニンの回路が完成します。この回路は活性型メチル基回路(Activated Methyl Cycle)と呼ばれます。活性型メチル基回路はメチル基の供与体である S-アデノシルメチオニンを生成するという点で重要な回路です。
ところで、5-メチルテトラヒドロ葉酸もメチル基転位を行う分子です。活性型メチル基回路は 5-メチルテトラヒドロ葉酸からメチル基を SAM に渡す回路と解釈できます。もともとメチル化を行う分子である 5-メチルテトラヒドロ葉酸からわざわざ SAM にメチル基を渡す必要があるのでしょうか?実は 5-メチルテトラヒドロ葉酸はそれほどメチル基を転位する能力が高くありません。様々な分子にメチル基を付加するにはもっと高いメチル基転位ポテンシャルを持つ分子(メチル基を転位する能力の高い分子)が必要となります。そこで、活性型メチル基回路ではより高いメチル基転位ポテンシャルを持つ SAM を生成して、様々な生合成経路でのメチル化に利用しています。このように、活性型メチル基回路ではより高いメチル基転位ポテンシャルを持つ SAM を供給する役割を担っています。
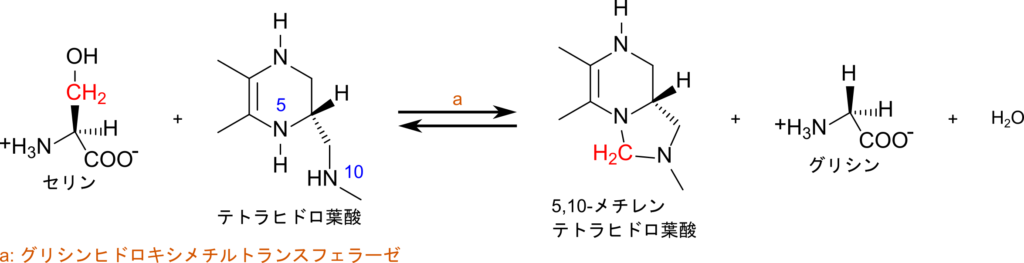
グリシンの生合成とテトラヒドロ葉酸
グリシンの生合成
グリシンの生合成はセリンからメチレン基を脱離することで行われます。この時にメチレン基の受容体として機能するのはテトラヒドロ葉酸です(図4)。
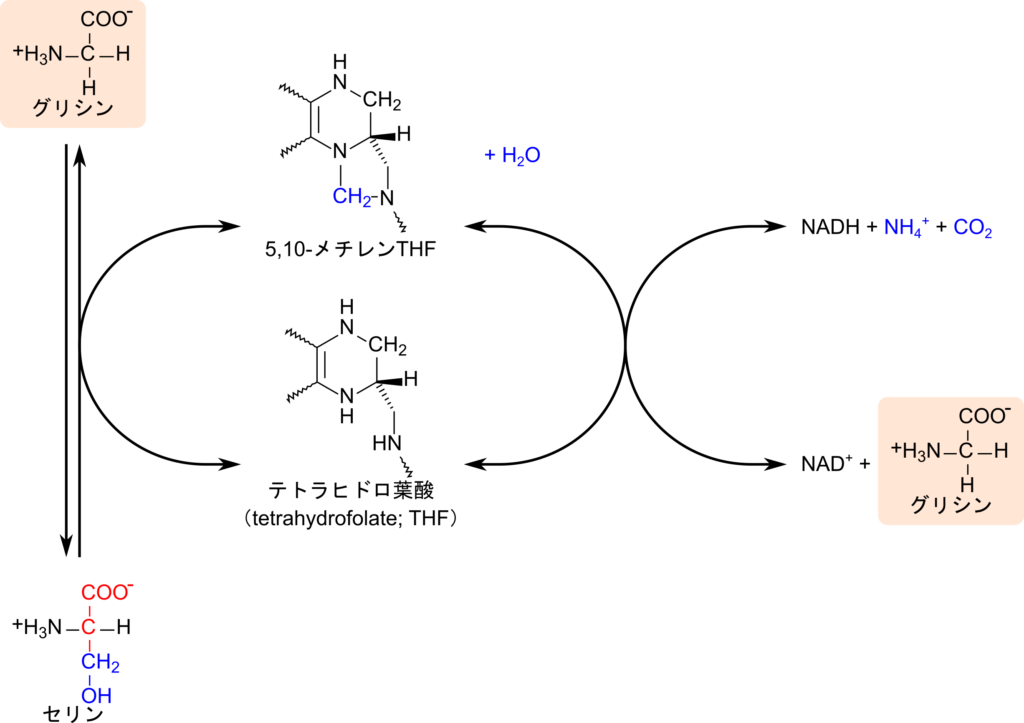
ところで、グリシンからメチレン基がテトラヒドロ葉酸に渡されるとともに酸化されるとアンモニウム塩と炭酸が生じてグリシンが分解されます。この反応はグリシン開裂系(Glycine cleavage system)として知られており、逆反応も進行可能です。逆反応が進んだ場合は以下のような反応となり、グリシンが生成されます。
CO2 + NH4+ + 5,10-メチレンテトラヒドロ葉酸 + NADH ⇆ グリシン + テトラヒドロ葉酸 + NAD+
テトラヒドロ葉酸と、その誘導体とグリシン生合成
グリシンの生合成についてテトラヒドロ葉酸に注目して考察してみましょう。まずセリン→グリシンの反応では、テトラヒドロ葉酸にメチレン基が渡されて、5,10-メチレンテトラヒドロ葉酸が生成されます。一方で、アンモニウム塩+炭酸→グリシンの反応では 5,10-メチレンテトラヒドロ葉酸が消費されてテトラヒドロ葉酸が再生されます。さらに、セリンは前述の通り、3-ホスホグリセリン酸から生成されますから、セリンから供給されたメチレン基は 3-ホスホグリセリン酸から供給されていることにもなります。したがって、セリンを介した 5,10-メチレンテトラヒドロ葉酸の生成は糖質から1炭素単位※(メチレン基)を供給する経路と解釈できます。
こうして産生された 5,10-メチレンテトラヒドロ葉酸は上述のようなグリシンの生成のほかにも dUMP から TMP の生成(こちらで紹介しています)など、メチレン基の転位反応に利用されるほか、5-メチルテトラヒドロ葉酸(メチル基 -CH3 の供与体)や 5,10-メテニルテトラヒドロ葉酸(メテニル基 -CH= の供与体)など様々な1炭素単位を供給する供与体を生成する中間体でもあります。
一方で、アンモニウム塩+炭酸→グリシンの生合成では 5,10-メチレンテトラヒドロ葉酸からテトラヒドロ葉酸を生成する役割を担っています。テトラヒドロ葉酸は様々な1炭素単位を受け取る受容体として機能します。
このように、グリシンの生合成経路(あるいは異化経路)はテトラヒドロ葉酸やその誘導体の生成に密接に関連しており、これらのテトラヒドロ葉酸やその誘導体は1炭素単位を供与したり除去する反応に関与しています。
※1炭素単位:炭素一つで構成される置換基の総称をいいます。テトラヒドロ葉酸は1炭素単位の受容体として機能し、その誘導体は1炭素単位の供与体として機能します。
例)ホルミル基(-CHO)、メチル基(-CH3)、メチレン基(-CH2-)、メテニル基(-CH=)
今回は、3-ホスホグリセリン酸から生合成されるアミノ酸について解説してきました。これらの経路は単にアミノ酸を合成するだけでなく、生体にとって極めて重要な一炭素単位の供給源としても機能しています。加えて、システインの生合成経路はメチオニンの異化経路と表裏一体となっているなど、その多機能性から生物の巧妙な設計が垣間見えます。
このように、セリン・グリシン・システインの生合成経路は一見シンプルでありながら、その背後には奥深い意味と驚きが隠されています。本記事では、そうした生合成経路の多機能性や意外性を理解できるよう心がけて書きしました。ぜひ、繰り返し読み返すことで、より深い理解と新たな気づきを得ていただければ嬉しく思います。
参考文献
- 島原健三 (1991). 概説 生物化学. 三共出版. pp. 208-223
- Jeremy M. Berg, John L. Tymoczko, Gregory J. Gatto Jr., Lubert Stryer著、入村達郎、岡山博人、清水孝雄、中野徹訳 (2018). ストライヤー生化学 第8版. 東京化学同人. pp.665-693
- D. Voet, J. G. Voet, C. W. Pratt 著、田宮信雄、八木達彦、遠藤斗志也、吉久徹訳 (2017) ボート 基礎生化学 第5版. 東京化学同人. pp.496-503
- KEGG PATHWAY DATABASE. 2025-03-03. https://www.genome.jp/kegg/pathway.html
- Lu, S. C., & Mato, J. M. (2012). S -adenosylmethionine in Liver Health, Injury, and Cancer. Physiological Reviews, 92(4), 1515–1542. https://doi.org/10.1152/physrev.00047.2011
- Ramanathan, A., Robb, G. B., & Chan, S. H. (2016, September 19). mRNA capping: Biological functions and applications. Nucleic Acids Research. Oxford University Press. https://doi.org/10.1093/nar/gkw551
- Lee, Y. H., Ren, D., Jeon, B., & Liu, H. W. (2023, March 9). S-Adenosylmethionine: more than just a methyl donor. Natural Product Reports. Royal Society of Chemistry. https://doi.org/10.1039/d2np00086e